
Wetenschap
Waarom explodeert natriumchloride in water?
Dit is waarom:
* oplossen, niet reageren: Wanneer natriumchloride aan water wordt toegevoegd, lost dit op. Dit betekent dat de ionische bindingen het natrium (Na+) en chloride (Cl-) ionen aan elkaar houden, en de ionen worden omringd door watermoleculen. Dit proces geeft warmte vrij, maar niet genoeg om een explosie te veroorzaken.
* Geen chemische reactie: Het oplossen van zout in water is een fysieke verandering, geen chemische reactie. Er zijn geen nieuwe stoffen gevormd, alleen een verandering in toestand van vaste tot opgeloste ionen.
* stabiele verbinding: Natriumchloride is een zeer stabiele verbinding. Het reageert niet gemakkelijk met water om explosieve producten te produceren.
misvattingen:
Het idee dat zout in water explodeert, kan voortkomen uit het verwarren met andere stoffen:
* Natriummetaal: Elementair natrium (NA) is zeer reactief met water. De reactie geeft een significante hoeveelheid warmte- en waterstofgas vrij, die kan ontsteken en een explosie kan veroorzaken.
* Natriumhypochloriet: Deze verbinding, vaak aangetroffen in bleekmiddel, kan reageren met zuren om chloorgas te produceren, wat giftig is en in bepaalde omstandigheden explosief kan zijn.
Conclusie:
Zout dat oplost in water is een veilig en gemeenschappelijk proces. Het is belangrijk om onderscheid te maken tussen natriumchloride (tafelzout) en andere stoffen die gevaarlijk kunnen reageren met water.
 Waterefficiëntie in landelijke gebieden wordt slechter, zelfs als het verbetert in stedelijke centra
Waterefficiëntie in landelijke gebieden wordt slechter, zelfs als het verbetert in stedelijke centra Antarctische subglaciale meren zijn koud, donker en vol geheimen
Antarctische subglaciale meren zijn koud, donker en vol geheimen NASA vindt sterkste stormen in verzwakkende tropische cycloon Sanba
NASA vindt sterkste stormen in verzwakkende tropische cycloon Sanba Preseismische atmosferische radonanomalie geassocieerd met aardbeving in Noord-Osaka in 2018
Preseismische atmosferische radonanomalie geassocieerd met aardbeving in Noord-Osaka in 2018 Laat me je bladeren zien – Gezondheidscontrole voor stadsbomen
Laat me je bladeren zien – Gezondheidscontrole voor stadsbomen
Hoofdlijnen
- Dragen axonen actiepotentialen weg van het cellichaam?
- Welke term wordt gebruikt om een chipmunk te beschrijven dat zaden of fruit eet?
- Waar worden eiwitten in alle cel gemaakt?
- Welke organel zou het meest talrijk zijn in de cellen van je mond?
- In welke theorie is Charles Darwin bekend?
- Onderzoek suggereert dat gorilla's spontaan voedselreinigingsgedrag kunnen ontwikkelen
- Schimmel is afhankelijk van bacteriën om de belangrijkste componenten van zijn voortplantingsmechanisme te reguleren
- Dode bomen leven met schimmels
- Welk organel is verantwoordelijk voor de afvalverwerking en recycling in een dierlijke cel?
- Wetenschap onthult geheimen van een mummieportret

- Nieuwe doorbraak in nanotechnologie die atmosferische koolstof gebruikt om nuttige chemicaliën te maken

- Kikkerschuim gebruiken als een antiseptisch toedieningssysteem

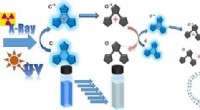
- Onzichtbare röntgenstralen worden blauw
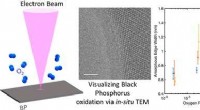
- Ingenieurs bevorderen inzichten over zwarte fosfor als materiaal voor toekomstige flexibele elektronica met ultralaag vermogen
 Wetenschappers laten zien hoe vrouwelijke gameten het herstel van de bevruchting in bloeiende planten regelen
Wetenschappers laten zien hoe vrouwelijke gameten het herstel van de bevruchting in bloeiende planten regelen  Hoe komt kalium de cellen binnen?
Hoe komt kalium de cellen binnen? Hoe vindt transpiratie plaats in levende organismen?
Hoe vindt transpiratie plaats in levende organismen?  Ideeën voor Cookie Science Fair Projects
Ideeën voor Cookie Science Fair Projects Hoeveel allels per gen zijn er in elke fase van meiose?
Hoeveel allels per gen zijn er in elke fase van meiose?  Wat is de waarde van versnelling als gevolg van zwaartekracht in de ruimte?
Wat is de waarde van versnelling als gevolg van zwaartekracht in de ruimte?  Hoe isotopen
Hoe isotopen Welke aanpassingen moeten de bevers overleven?
Welke aanpassingen moeten de bevers overleven?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

