
Wetenschap
Ionisch of covalent? De binding in ijzersulfide (FeS) begrijpen
* Verschil in elektronegativiteit: IJzer (Fe) heeft een elektronegativiteit van 1,83, terwijl zwavel (S) een elektronegativiteit van 2,58 heeft. Het verschil in elektronegativiteit is significant (0,75), wat wijst op een sterke neiging van zwavel om elektronen uit ijzer aan te trekken.
* Metaal en niet-metaal: IJzer is een metaal en zwavel is een niet-metaal. Metalen hebben de neiging elektronen te verliezen en kationen te vormen, terwijl niet-metalen de neiging hebben elektronen te winnen en anionen te vormen.
* Vorming van ionen: In FeS verliest ijzer twee elektronen om Fe²⁺ (ijzer(II)-ion) te vormen, en zwavel krijgt twee elektronen om S²⁻ (sulfide-ion) te vormen.
Daarom is de sterke elektrostatische aantrekkingskracht tussen de tegengesteld geladen ionen (Fe²⁺ en S²⁻) het bepalende kenmerk van een ionische binding in FeS.
 Materiaalonderzoek onderzoekt ontwerpregels en synthese van kandidaten voor kwantumgeheugen
Materiaalonderzoek onderzoekt ontwerpregels en synthese van kandidaten voor kwantumgeheugen  U kunt zien of een mengsel oplossing of ophanging is wanneer u?
U kunt zien of een mengsel oplossing of ophanging is wanneer u?  Welk gas ontstaat wanneer aluminium reageert met natriumhydroxide?
Welk gas ontstaat wanneer aluminium reageert met natriumhydroxide?  Voorbeeld van een filtering vaste stof uit gas?
Voorbeeld van een filtering vaste stof uit gas?  In de reactie geeft FeCl2 plus 2NAOH IJs II Hydroxide 2Nacl 6 Mol Mol van worden toegevoegd aan NaOH Hoeveel zouden er in reactie worden opgebruikt?
In de reactie geeft FeCl2 plus 2NAOH IJs II Hydroxide 2Nacl 6 Mol Mol van worden toegevoegd aan NaOH Hoeveel zouden er in reactie worden opgebruikt?
Hoofdlijnen
- Wat is de enige taxonomische categorie die bestaat als een discrete eenheid in de natuur?
- In zaadplanten wordt de structuur die de mannelijke gametofyt omsluit en naar een andere plant transporteert een?
- Wat zijn de verschillen tussen een typische dierlijke cel en een dermiscel?
- Waarom denken wetenschappers dat introns en exons bijdragen aan evolutionaire flexibiliteit?
- Vroegste gibbonfossiel gevonden in het zuidwesten van China
- Mysterie van uitgestorven Nieuw-Zeelandse vissen ontrafeld
- Is het volgende waar of niet waar de voorouder van alle eukaryotische cellen ongeveer 2 miljard jaar geleden evolueerde?
- Hoe bewegen onze cellen? Vloeistofdruppels zouden dit kunnen verklaren
- Onderzoekers onderzoeken systematisch de werkzaamheid van CRISPR-antimicrobiële middelen
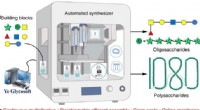
- Geautomatiseerde koolhydraatsynthesizer produceert polysachariden met een recordlengte
- Iowa's recordkoude temperaturen:een historisch overzicht

- Eindelijk, het antwoord op een brandende vraag van 40 jaar

- Wetenschappers gebruiken trechtervisie om goedkope en efficiënte zonne-energie te pionieren

- Sleutel tot koolstofvrije auto's? Kijk naar de sterren

 Radius vinden op basis van Diameter
Radius vinden op basis van Diameter Nieuwe furore op Facebook-privacy:wat staat er op het spel?
Nieuwe furore op Facebook-privacy:wat staat er op het spel? Hoe komt energie het aardsysteem binnen van interne bronnen door convectie en externe stralingzon?
Hoe komt energie het aardsysteem binnen van interne bronnen door convectie en externe stralingzon?  In welke vorm bestaat salpeterzuur?
In welke vorm bestaat salpeterzuur?  Wat is de golflengte met een energie van 510?
Wat is de golflengte met een energie van 510?  Acht binaire milliseconde pulsars onderzocht door onderzoekers
Acht binaire milliseconde pulsars onderzocht door onderzoekers Schietpartij op school in Texas:hoe geweren en munitie in aanvalsstijl verminking doden
Schietpartij op school in Texas:hoe geweren en munitie in aanvalsstijl verminking doden  Als een populatie van rupsen zich voedt met de bladerenbomen in het bos en voedsel voor vogels draait die ze opeten, welke aanpassing zou het meest waarschijnlijk evolueren?
Als een populatie van rupsen zich voedt met de bladerenbomen in het bos en voedsel voor vogels draait die ze opeten, welke aanpassing zou het meest waarschijnlijk evolueren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

