
Wetenschap
Basisgedrag in oplossing begrijpen:voorbij ionisatie
Hier is een duidelijkere manier om erover na te denken:
* Zuren: In oplossing doneren zuren protonen (H⁺) aan de omringende watermoleculen. Dit verhoogt de concentratie van H⁺-ionen, waardoor de oplossing zuur wordt.
* Basis: In oplossing kunnen basen:
* Accepteer protonen: Dit is de meest gebruikelijke manier waarop bases werken. Ze reageren met H⁺-ionen, verwijderen ze uit de oplossing en verlagen de zuurgraad. Dit proces wordt neutralisatie genoemd .
* Doneer hydroxide-ionen (OH⁻): Sterke basen zoals NaOH (natriumhydroxide) geven OH⁻-ionen direct af in oplossing. Deze ionen reageren vervolgens met H⁺-ionen uit watermoleculen, waardoor de OH⁻-concentratie verder toeneemt en de oplossing basisch wordt.
Belangrijke opmerking: Hoewel zowel zuren als basen in oplossing ioniseren, bepalen hun effecten op de concentratie van H⁺- en OH⁻-ionen hun zuurgraad of basiciteit.
Laat het me weten als je meer details wilt over hoe verschillende bases werken!
 Vulkaan Indonesië braakt enorme askolom uit
Vulkaan Indonesië braakt enorme askolom uit Een op de zes historische bronnen in Colorado bevindt zich in een overstromingsgebied
Een op de zes historische bronnen in Colorado bevindt zich in een overstromingsgebied Welke invloed heeft uw omgeving op de voedselkeuze?
Welke invloed heeft uw omgeving op de voedselkeuze?  Alle bladverliezende bomen verliezen hun bladeren Deze boom is een verlies, wat beschrijven deze?
Alle bladverliezende bomen verliezen hun bladeren Deze boom is een verlies, wat beschrijven deze?  Wat is de op een na grootste bron van zwaartekracht?
Wat is de op een na grootste bron van zwaartekracht?
Hoofdlijnen
- Zijn bacteriën een bron van restrictie -enzymen in DNA?
- Neutronen onthullen hoe het pancratistatine op kanker jaagt en gezonde cellen in stand houdt
- Welke selectieve groeimedia is het meest geschikt voor het isoleren van coliforme bacteriën?
- Hoe was de manier van denken verbonden met de wetenschappelijke methode?
- Wat zijn de factoren die de groei en deling van cellen regelen?
- Onderzoek toont aan dat zachtere eiwitten sneller de kern kunnen binnendringen
- Welke endocriene klier bevindt zich in de luchtpijp?
- Wat zijn de bases van het classificeren van organismen?
- Zijn gameten in schimmels of mitose?
- Is azijn een betrouwbaar spinnenafweermiddel? Inzichten uit recent onderzoek

- Kunstmatige enzymfuncties evenals natuurlijke versie
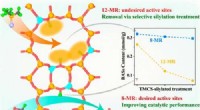
- Nieuwe strategie om de verspreiding van zuurplaatsen in zeolieten te beheersen
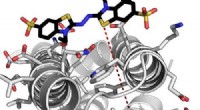
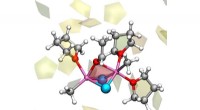
- De 120 jaar oude cold case voor de Grignard-reactie is eindelijk opgelost
- Duurzamere omzetting van aminozuren met licht in plaats van met warmte

 Welke thermische energie zou het snelst overbrengen door een vaste stof?
Welke thermische energie zou het snelst overbrengen door een vaste stof?  Welke materialen zijn slechte reflectoren?
Welke materialen zijn slechte reflectoren?  Micropopulisme maakt van onderwijs misschien een slagveld in de cultuuroorlogen
Micropopulisme maakt van onderwijs misschien een slagveld in de cultuuroorlogen Cellulaire entropie:wanorde en levensprocessen begrijpen
Cellulaire entropie:wanorde en levensprocessen begrijpen  Welke deeltjes worden samengesmolten in de zon om energie te produceren?
Welke deeltjes worden samengesmolten in de zon om energie te produceren?  Leg uit hoe rotsfragmenten kunnen worden gesorteerd op maat op een strand?
Leg uit hoe rotsfragmenten kunnen worden gesorteerd op maat op een strand?  Wat is het verschil tussen evolutietheorie en biologische evolutie?
Wat is het verschil tussen evolutietheorie en biologische evolutie?  Hoeveel mol kaliumhydroxide is vereist om een oplossing van 300 ml 0,250 m te bereiden?
Hoeveel mol kaliumhydroxide is vereist om een oplossing van 300 ml 0,250 m te bereiden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

