
Wetenschap
Ontleding van zuiveringszout:productgrammen berekenen
1. Evenwichtige chemische vergelijking:
De ontleding van zuiveringszout wordt weergegeven door de volgende uitgebalanceerde chemische vergelijking:
2 NaHCO₃(s) → Na₂CO₃(s) + H₂O(g) + CO₂(g)
Deze vergelijking vertelt ons dat 2 mol natriumbicarbonaat (NaHCO₃) uiteenvalt en 1 mol natriumcarbonaat (Na₂CO₃), 1 mol water (H₂O) en 1 mol kooldioxide (CO₂) produceert.
2. Molaire massa's:
* NaHCO₃ (zuiveringszout):84,01 g/mol
* Na₂CO₃ (natriumcarbonaat):105,99 g/mol
* H₂O (water):18,02 g/mol
* CO₂ (kooldioxide):44,01 g/mol
3. Stoichiometrieberekeningen:
* Stap 1:Molletje zuiveringszout:
Converteer de massa zuiveringszout (42,0 g) naar mol met behulp van de molaire massa:
mol NaHCO₃ =(42,0 g) / (84,01 g/mol) =0,500 mol
* Stap 2:mollen producten:
Gebruik de molverhoudingen uit de uitgebalanceerde vergelijking om het aantal mol van elk product te vinden:
* mol Na₂CO₃ =(0,500 mol NaHCO₃) * (1 mol Na₂CO₃ / 2 mol NaHCO₃) =0,250 mol
* mol H₂O =(0,500 mol NaHCO₃) * (1 mol H₂O / 2 mol NaHCO₃) =0,250 mol
* mol CO₂ =(0,500 mol NaHCO₃) * (1 mol CO₂ / 2 mol NaHCO₃) =0,250 mol
* Stap 3:Gram producten:
Converteer de mollen van elk product naar grammen met behulp van hun respectievelijke molmassa's:
* gram Na₂CO₃ =(0,250 mol) * (105,99 g/mol) =26,5 g
* gram H₂O =(0,250 mol) * (18,02 g/mol) =4,51 g
* gram CO₂ =(0,250 mol) * (44,01 g/mol) =11,0 g
Daarom:
* 26,5 gram natriumcarbonaat (Na₂CO₃) geproduceerd.
* 4,51 gram water (H₂O) geproduceerd.
* 11,0 gram kooldioxide (CO₂) geproduceerd.
 Waarom geeft een micro-organisme uit Yellowstone de voorkeur aan magere rantsoenen boven rijke?
Waarom geeft een micro-organisme uit Yellowstone de voorkeur aan magere rantsoenen boven rijke?  Waarom moessons zeer pulserend van aard zijn?
Waarom moessons zeer pulserend van aard zijn?  Klimaatverandering zorgt ervoor dat de moessons in India grillig zijn. Kunnen boeren nog steeds een manier vinden om te floreren?
Klimaatverandering zorgt ervoor dat de moessons in India grillig zijn. Kunnen boeren nog steeds een manier vinden om te floreren?  Wereldwijd onderzoek toont aan dat milieuvriendelijke landbouw de productiviteit kan verhogen
Wereldwijd onderzoek toont aan dat milieuvriendelijke landbouw de productiviteit kan verhogen Hoe is kennis van fysieke geografie nuttig voor een weersvoorspeller?
Hoe is kennis van fysieke geografie nuttig voor een weersvoorspeller?
Hoofdlijnen
- Nieuwe ontdekking om de ontwikkeling van zouttolerante wijnstokken te versnellen
- Hoe stijgen en zinken vissen in het water?
- Wat zorgt ervoor dat plantenwortels naar de zwaartekracht toe groeien? Onderzoek identificeert vier genen
- Biofysici onthullen hoe drie eiwitten samenwerken om de cellulaire beweging te verfijnen
- In de meeste meercellige organismen worden cellen georganiseerd volgens hun?
- De soorten planten die in een bioom worden gevonden, worden voornamelijk bepaald door?
- Welke twee uitspraken verklaren hoe de orgaansystemen van een regenworm de cellen van zuurstof helpen voorzien?
- De twee belangrijkste manieren waarop neuronen in staat zijn om stimuli te reageren?
- De cruciale rol van thylakoïden:schijfachtige structuren die de fotosynthese aandrijven
- Open-sourcesoftware verwerkt snel spectrale gegevens, identificeert en kwantificeert nauwkeurig lipidensoorten

- Bouw een 3D-Bohr-model:een praktische gids voor atomaire structuur

- Vis kan helpen bij het zoeken naar medicijnen tegen multiple sclerose
- Bedwelmend lichtgevoelig
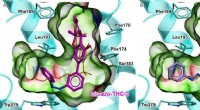
- Onderzoekers triggeren enzymen met licht
 Wat is de lichaamssymmetrie van leverblees?
Wat is de lichaamssymmetrie van leverblees?  Wat zijn de versnellingsrechten voor de zwaartekracht nabij het oppervlak van de aarde?
Wat zijn de versnellingsrechten voor de zwaartekracht nabij het oppervlak van de aarde?  Onderzoek onthult ontbrekende fysica in explosieve hotspots
Onderzoek onthult ontbrekende fysica in explosieve hotspots Wetenschappers ontslagen van EPA Forge Ahead met onofficieel rapport over verontreinigende stoffen
Wetenschappers ontslagen van EPA Forge Ahead met onofficieel rapport over verontreinigende stoffen  De eigenschappen van vaste stoffen, vloeistoffen en gassen
De eigenschappen van vaste stoffen, vloeistoffen en gassen  Onderzoekers ontwikkelen chemie die nodig is om marihuana-ademtester te maken
Onderzoekers ontwikkelen chemie die nodig is om marihuana-ademtester te maken Hoe ontstaan sferoïdale keien?
Hoe ontstaan sferoïdale keien?  Gebrek aan betaalbare huur plaagt steden in de Verenigde Staten
Gebrek aan betaalbare huur plaagt steden in de Verenigde Staten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

