
Wetenschap
Beryllium en calcium:hun vergelijkbare chemische eigenschappen begrijpen
Dit is waarom dit belangrijk is:
* Reactiviteit: Het hebben van twee valentie-elektronen betekent dat ze deze elektronen gemakkelijk verliezen om +2 kationen te vormen. Dit maakt ze zeer reactief, vooral met niet-metalen zoals zuurstof en halogenen.
* Verbinding: De neiging om +2 ionen te vormen leidt tot ionische binding met niet-metalen, resulterend in de vorming van ionische verbindingen zoals oxiden, chloriden en sulfaten.
* Metallic karakter: Zowel beryllium als calcium zijn metalen en vertonen karakteristieke eigenschappen zoals glans, kneedbaarheid en geleidbaarheid.
Er zijn echter enkele verschillen in hun reactiviteit vanwege:
* Atomische grootte: Calcium is groter dan beryllium, wat betekent dat de valentie-elektronen zich verder van de kern bevinden en gemakkelijker te verwijderen zijn. Dit maakt calcium reactiever dan beryllium.
* Elektronegativiteit: Calcium is minder elektronegatief dan beryllium, wat betekent dat het waarschijnlijker zijn elektronen verliest.
Hoewel beryllium en calcium vergelijkbare chemische eigenschappen delen vanwege hun vergelijkbare elektronenconfiguraties, variëren hun reactiviteit en andere eigenschappen over het algemeen als gevolg van verschillen in hun atomaire grootte en elektronegativiteit.
 De impact van klimaatverandering in droge en warme periodes in de Pyreneeën
De impact van klimaatverandering in droge en warme periodes in de Pyreneeën Om erachter te komen hoe het met de natuur gaat, proberen wetenschappers te luisteren
Om erachter te komen hoe het met de natuur gaat, proberen wetenschappers te luisteren  Verschil tussen mannelijke en vrouwelijke sprinkhanen
Verschil tussen mannelijke en vrouwelijke sprinkhanen  Wat is milieugeografie voor kinderen?
Wat is milieugeografie voor kinderen?  Kan het wassen van onze kleding met wasmiddel tot het verleden behoren?
Kan het wassen van onze kleding met wasmiddel tot het verleden behoren?
Hoofdlijnen
- Verschillen en overeenkomsten tussen Unicellular & Cellular
- In de cel:hoe ADP ATP wordt via mitochondriale chemiosmose
- Belangrijke orgaansystemen die de menselijke homeostase in stand houden
- Welke voedingsmiddelen zijn macromoleculen?
- Waar zijn de genetische materialenchromosomen opgeslagen in planten- en dierlijke cel?
- Wat betekent primitief in biologie?
- De RNA -soorten die de gecodeerde boodschap draagt die sequentie van aminozuren in eiwit specificeert te maken van nuclueus cytoplasma is?
- Wat is de nuttige actie van schimmels?
- Wie concludeerde dat alle planten bestaan uit levende cellen?
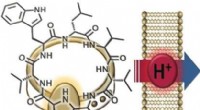
- Chemische synthese toont aan dat antibioticum uit de menselijke neus werkt door protontranslocatie
- Zeer efficiënte waterstofgasproductie met behulp van zonlicht, water en hematiet

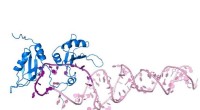
- Nieuw inzicht in de rijping van miRNA's
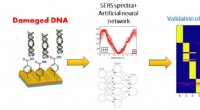
- Onderzoekers zorgen ervoor dat neurale netwerken met succes DNA-schade door UV-straling detecteren
- Nieuwe fotogevoelige hydrogels ontwikkeld met oog voor biomedische toepassingen

 Welke energie verandert er in een elektrisch ijzer?
Welke energie verandert er in een elektrisch ijzer?  Wat drijft de enorme bloemen van bruin zeewier die zich opstapelen op de stranden van Florida en de Caraïben?
Wat drijft de enorme bloemen van bruin zeewier die zich opstapelen op de stranden van Florida en de Caraïben? Wat zijn de eenheden van een beker en wat meet het?
Wat zijn de eenheden van een beker en wat meet het?  Amerikaanse astronauten beginnen op 3 oktober aan ruimtewandeling om ISS-robotarm te repareren
Amerikaanse astronauten beginnen op 3 oktober aan ruimtewandeling om ISS-robotarm te repareren Spanje, Portugal kampt met extreme droogte
Spanje, Portugal kampt met extreme droogte Is basalt foliated of niet -foliated?
Is basalt foliated of niet -foliated?  Jordanië kampt zomer met watertekorten
Jordanië kampt zomer met watertekorten Hoe je toch een resistente parasiet kunt doden
Hoe je toch een resistente parasiet kunt doden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

