
Wetenschap
Hydrofobiciteit begrijpen:de meest waterafstotende moleculen identificeren
* Perfluorkoolwaterstoffen (PFK's): Dit zijn verbindingen die alleen koolstof- en fluoratomen bevatten. De hoge elektronegativiteit van fluor creëert een zeer sterke niet-polaire binding met koolstof, waardoor PFC's extreem hydrofoob worden. Voorbeelden zijn onder meer perfluoroctaan (C8F18) en perfluordecaline (C10F18).
* Verzadigde koolwaterstoffen: Deze moleculen bestaan alleen uit koolstof- en waterstofatomen die met elkaar verbonden zijn door enkele bindingen. Ze missen polaire groepen en zijn daarom zeer hydrofoob. Voorbeelden zijn onder meer methaan (CH4), ethaan (C2H6) en hexaan (C6H14).
* Alifatische ketens: Lange ketens van koolstof- en waterstofatomen, gebruikelijk in vetten en oliën, zijn over het algemeen hydrofoob.
Het is belangrijk op te merken dat:
* Hydrofobiciteit is een spectrum: Er is geen duidelijke lijn die moleculen verdeelt in 'hydrofoob' en 'hydrofiel'. In plaats daarvan vertonen moleculen een reeks hydrofobiciteiten.
* Hydrofobiciteit is contextafhankelijk: De hydrofobiciteit van een molecuul kan worden beïnvloed door factoren zoals het oplosmiddel waarin het zich bevindt, de temperatuur en de aanwezigheid van andere moleculen.
Hoewel PFC's en verzadigde koolwaterstoffen tot de meest hydrofobe moleculen behoren, is het dus niet mogelijk om één enkel molecuul 'meest hydrofoob' te noemen zonder de context te specificeren.
 Hoe hebben mensen de gematigde bossen positief en negatief beïnvloed?
Hoe hebben mensen de gematigde bossen positief en negatief beïnvloed?  Eiken in plaats van palmbomen? De iconische palmen van Florida snijden het niet met klimaatverandering
Eiken in plaats van palmbomen? De iconische palmen van Florida snijden het niet met klimaatverandering Vulkaan in het zuiden van Japan barst uit; geen verwondingen of schade
Vulkaan in het zuiden van Japan barst uit; geen verwondingen of schade Zijn waterjuffers in nood?
Zijn waterjuffers in nood?  Hawaï vulkaanlava vernietigt honderden huizen 's nachts
Hawaï vulkaanlava vernietigt honderden huizen 's nachts
Hoofdlijnen
- Hoe heet elk individuele chromosomen?
- MRI laat zien hoe kroonrotinfectie bij aardbeien verloopt
- Welk belang zijn buffers voor levende organismen?
- Welke biomen zijn er in Europa?
- Wat zijn de structuren voor een nucleïnezuur?
- Laat me je bladeren zien - Gezondheidscontrole voor stadsbomen
- Wat is de hyoid?
- Wat is de wetenschapsapparaat?
- Zie hoe ze groeien:afzonderlijke bacteriën monitoren zonder microscoop
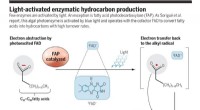
- Een algenfoto-enzym dat blauw licht gebruikt om vetzuren om te zetten in koolwaterstoffen
- Het beheersen van molverhoudingen:van empirische formules tot gebalanceerde vergelijkingen

- Blad-pH en fotosynthese:inzicht in de optimale zuurgraad van RuBisCO

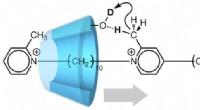
- Moleculaire machine maakt gebruik van beweging in één richting
- Bouw uw eigen aquariumopvangbak:een stapsgewijze handleiding

 Hoe weet een bacterie dat het tijd is om zich te splitsen?
Hoe weet een bacterie dat het tijd is om zich te splitsen?  Quantum dots houden atomen op afstand om katalyse te stimuleren
Quantum dots houden atomen op afstand om katalyse te stimuleren Wat zijn voorbeelden van elastische voorjaarskracht?
Wat zijn voorbeelden van elastische voorjaarskracht?  Welk proces veroorzaakt evolutie?
Welk proces veroorzaakt evolutie?  Vlamontwerp in de ruimte kan leiden tot roetvrij vuur
Vlamontwerp in de ruimte kan leiden tot roetvrij vuur Hoe krijgt Neon zijn kleuren?
Hoe krijgt Neon zijn kleuren?  Welke bries waait in een berg-valley-systeem?
Welke bries waait in een berg-valley-systeem?  Onderzoeksteam ontwikkelt recordlaser op chip
Onderzoeksteam ontwikkelt recordlaser op chip
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

