
Wetenschap
Elektrostatische aantrekkingskracht in moleculen begrijpen:ionische en polaire bindingen
Hier is een overzicht:
* Polaire covalente obligaties: In veel moleculen zijn elektronen niet gelijk verdeeld tussen atomen. Deze ongelijke verdeling creëert een gedeeltelijke positieve lading (δ+) op het ene atoom en een gedeeltelijke negatieve lading (δ-) op het andere. Dit wordt een polaire covalente binding genoemd .
* Elektrostatische aantrekkingskracht: De tegengestelde ladingen (δ+ en δ-) binnen het molecuul trekken elkaar aan. Deze aantrekkingskracht is elektrostatisch van aard, vergelijkbaar met de aantrekkingskracht tussen magneten met tegengestelde polen.
* Intramoleculaire binding: Deze aantrekking vindt plaats *binnen* hetzelfde molecuul, wat bijdraagt aan de algehele stabiliteit en structuur van het molecuul.
Voorbeeld:
Beschouw het watermolecuul (H₂O):
* Zuurstof is elektronegatiever dan waterstof, wat betekent dat het sterker elektronen aantrekt.
* Dit leidt tot een gedeeltelijke negatieve lading (δ-) op het zuurstofatoom en gedeeltelijke positieve ladingen (δ+) op de waterstofatomen.
* De elektrostatische aantrekkingskracht tussen de δ+ waterstofatomen en het δ-zuurstofatoom helpt het watermolecuul bij elkaar te houden.
Andere belangrijke punten:
* Ionische bindingen: Wanneer het verschil in elektronegativiteit tussen twee atomen erg groot is, kan het ene atoom een elektron volledig overdragen aan het andere. Hierdoor ontstaat een volledige positieve lading op het ene atoom en een volledig negatieve lading op het andere. De sterke aantrekkingskracht tussen deze tegengesteld geladen ionen wordt een ionische binding genoemd .
* Waterstofbinding: Een speciaal soort elektrostatische aantrekking vindt plaats wanneer een waterstofatoom gebonden is aan een zeer elektronegatief atoom (zoals zuurstof of stikstof). Hierdoor ontstaat er een sterke aantrekkingskracht tussen het waterstofatoom en een eenzaam elektronenpaar op een ander elektronegatief atoom. Dit wordt waterstofbinding genoemd en is een cruciale kracht in veel biologische systemen.
Samenvattend is de aantrekkingskracht tussen een positief geladen atoom en een negatief geladen atoom binnen hetzelfde molecuul het gevolg van elektrostatische krachten. Deze aantrekkingskracht draagt bij aan de structuur, stabiliteit en eigenschappen van het molecuul.
 Hoe verhouden de snelheden van voorwaartse en omgekeerde reacties zich bij een dynamisch chemisch evenwicht van de staat?
Hoe verhouden de snelheden van voorwaartse en omgekeerde reacties zich bij een dynamisch chemisch evenwicht van de staat?  Wat is de oplossing voor emissies?
Wat is de oplossing voor emissies?  Is salpeterzuur een organisch zuur?
Is salpeterzuur een organisch zuur?  Onderzoekers creëren een paradigmaverschuiving in de categorisatie van actieve locaties van katalysatoren, waardoor deuren worden geopend naar nieuw katalysatorontwerp
Onderzoekers creëren een paradigmaverschuiving in de categorisatie van actieve locaties van katalysatoren, waardoor deuren worden geopend naar nieuw katalysatorontwerp  Onderzoekers ontwikkelen milieuvriendelijke magneet om microplastics te bestrijden
Onderzoekers ontwikkelen milieuvriendelijke magneet om microplastics te bestrijden
 Hoe beïnvloeden mensen het naaldbos?
Hoe beïnvloeden mensen het naaldbos?  De helft van 's werelds jaarlijkse neerslag valt in slechts 12 dagen, nieuwe studie vondsten
De helft van 's werelds jaarlijkse neerslag valt in slechts 12 dagen, nieuwe studie vondsten Wat zijn de dingen die op aarde aanwezig zijn?
Wat zijn de dingen die op aarde aanwezig zijn?  Hoe wordt kooldioxide geabsorbeerd tijdens fotosynthese?
Hoe wordt kooldioxide geabsorbeerd tijdens fotosynthese?  Welke eigenschap van materie zou u waargenomen door uw Sense Touch te gebruiken?
Welke eigenschap van materie zou u waargenomen door uw Sense Touch te gebruiken?
Hoofdlijnen
- Wat verklaring geldt voor zowel mitose als meiose?
- Eiwitarm dieet in het vroege leven verlengt de levensduur van fruitvliegen
- Zoekers in Mexico vinden, maar laat los, vaquita bruinvis kalf
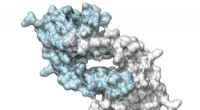
- Lussen, lussen en nog eens lussen:dit is hoe je DNA wordt georganiseerd
- Wat betekent anker in de biologie?
- Allelen:genvariaties en eigenschappen begrijpen
- Wat is de definitie van diafragma in samengestelde microscoop?
- Bacteriën en virussen hebben geen kern. Wat helpt hen om zich te voortplanten?
- Dode vissen en depressies aan de oevers van de Oder
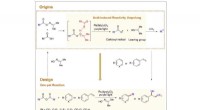
- Designer-enzym gebruikt onnatuurlijk aminozuur voor katalyse
- Softwarebibliotheek voor snellere verwerking van chemische reacties

- Efficiënte methode voor fotokatalytische fluoralkyleringen van (hetero)arenen
- Team ontwikkelt milieuvriendelijke, vlamvertragend koolstofplastic, ideaal voor recycling

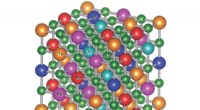
- Ongeordende materialen kunnen het moeilijkst zijn, meest hittebestendige carbiden
 Met een miljard gebruikers, Instagram neemt YouTube op in video (update)
Met een miljard gebruikers, Instagram neemt YouTube op in video (update) Waarom trekt de zon geen maan aan?
Waarom trekt de zon geen maan aan?  Welke wetenschappelijke discipline omvat de studie van aardbevingen?
Welke wetenschappelijke discipline omvat de studie van aardbevingen?  Bergen maken van kartonnen dozen
Bergen maken van kartonnen dozen  Hoe worden gegoten fossielen gevormd?
Hoe worden gegoten fossielen gevormd?  Dakgoten wemelen van onopvallend leven
Dakgoten wemelen van onopvallend leven Welke informatie onthult het potentiële energiediagram een reactie?
Welke informatie onthult het potentiële energiediagram een reactie?  Welk type energie wordt gedragen in fotonen?
Welk type energie wordt gedragen in fotonen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

