
Wetenschap
Het beheersen van molverhoudingen:van empirische formules tot gebalanceerde vergelijkingen
Door Chris Deziel | Bijgewerkt op 24 maart 2022
Op het gebied van de stoichiometrie – waar scheikundigen de relatieve hoeveelheden stoffen in reacties vergelijken – is het essentieel om te weten hoe de molverhouding moet worden bepaald. Of je nu de empirische formule van een onbekende verbinding uitwerkt of de precieze hoeveelheden reactanten en producten in een reactie berekent, de principes zijn hetzelfde:identificeer de eenvoudigste gehele getalsrelatie tussen de betrokken soort.
Een empirische formule bepalen
Wanneer een mysterieuze verbinding wordt geanalyseerd op zijn elementaire samenstelling, meet je meestal de massa van elk aanwezig element. Door deze massa's om te zetten in mol (massa ÷ atoomgewicht) wordt zichtbaar hoeveel mol van elk element er bestaat. Van daaruit kun je de eenvoudigste verhouding van gehele getallen afleiden:de empirische formule.
- Bereken het aantal mol van elk element. Deel de gemeten massa door het atoomgewicht van het element. Een verbinding die bijvoorbeeld 0,675 g H, 10,8 g O en 13,5 g Ca bevat, levert het volgende op:
- H:0,675 g ÷ 1,01 gmol⁻¹ =0,675 mol
- O:10,8 g ÷ 16,00 gmol⁻¹ =0,675 mol
- Ca:13,5 g ÷ 40,08 gmol⁻¹ =0,337 mol
- Delen door de kleinste molwaarde. Hier is Ca (0,337mol) het kleinst. Het delen van elke molwaarde door 0,337 geeft:
- H:0,675 ÷ 0,337 ≈ 2
- O:0,675 ÷ 0,337 ≈ 2
- Ca:0,337 ÷ 0,337 =1
- Schrijf de empirische formule op. De resulterende gehele getalsverhoudingen worden subscripts:CaO₂H₂, doorgaans uitgedrukt als Ca(OH)₂.
Een reactievergelijking in evenwicht brengen
Wanneer de reactanten en producten van een reactie bekend zijn, kunt u een onevenwichtige vergelijking schrijven en deze vervolgens in evenwicht brengen door de stoichiometrische coëfficiënten aan te passen. Deze coëfficiënten zijn in feite de molverhoudingen die voldoen aan de wet van behoud van massa.
- Begin met de onevenwichtige vergelijking. Bijvoorbeeld:H₂ + O₂ → H₂O.
- Breng de atomen in evenwicht. Vermenigvuldig elke zijde met de kleinste reeks gehele getallen die gelijk is aan het aantal atomen voor elk element. De uitgebalanceerde vergelijking wordt:2H₂ + O₂ → 2H₂O.
- Interpreteer de molverhoudingen. Uit de coëfficiënten:
- Waterstof naar zuurstof:2molH₂ :1molO₂ → 2:1
- Zuurstof naar water:1molO₂ :2molH₂O → 1:2
- Water naar waterstof:2molH₂O:4molH₂ → 1:2 (vereenvoudigd)
Deze coëfficiënten brengen niet alleen de vergelijking in evenwicht, maar vertellen je ook hoeveel mol van elke soort aan de reactie deelneemt. Het beheersen van deze techniek zorgt voor nauwkeurige stoichiometrische berekeningen voor elk chemisch proces.
 Engineered microbe kan de sleutel zijn tot het produceren van plastic uit planten
Engineered microbe kan de sleutel zijn tot het produceren van plastic uit planten Wat is de vergelijking voor zuurdissociatie -constante KA van koolzuur?
Wat is de vergelijking voor zuurdissociatie -constante KA van koolzuur?  Principes van stoomdestillatie
Principes van stoomdestillatie  Vastestofkatalyse:fluctuaties maken de weg vrij
Vastestofkatalyse:fluctuaties maken de weg vrij Hoe worden chemische vergelijkingen in evenwicht gebracht door de subscripts van moleculen waar of onwaar te veranderen?
Hoe worden chemische vergelijkingen in evenwicht gebracht door de subscripts van moleculen waar of onwaar te veranderen?
 Klimaatverandering kan lenen duurder maken voor staten en steden
Klimaatverandering kan lenen duurder maken voor staten en steden 'Elegante' oplossing onthult hoe het universum aan zijn structuur kwam
'Elegante' oplossing onthult hoe het universum aan zijn structuur kwam  Toen Billy door het bos wandelde, vond Billy een plant die hij nog nooit had gezien dat hij het type van wat de veiligste manier was, wilde identificeren, doe dit dan?
Toen Billy door het bos wandelde, vond Billy een plant die hij nog nooit had gezien dat hij het type van wat de veiligste manier was, wilde identificeren, doe dit dan?  Brexit bedreigt klimaatactie van de EU, uit onderzoek blijkt
Brexit bedreigt klimaatactie van de EU, uit onderzoek blijkt Onderzoek naar koolstofcycli in bosbodems gepresenteerd
Onderzoek naar koolstofcycli in bosbodems gepresenteerd
Hoofdlijnen
- Is het malaria gerelateerd aan natuurlijke selectie?
- Welk woord einde wordt geassocieerd met enzymen ASE en OSE?
- Is hennep hetzelfde als marihuana?
- Onderzoek naar hoe bacteriën bewegen, kan onderzoekers helpen antibacteriële oppervlakken te ontwikkelen
- Wat is de wetenschappelijke naam of taxonomische classificatie van plantentarwe?
- Wat verwijst Drosophila naar de classificatiegroep?
- Hoe zou jij het menselijk skelet definiëren?
- Wat is de wetenschappelijke naam voor wortels?
- Wat is Ribonucleic Acid?
- Tweefasig materiaal met verrassende eigenschappen

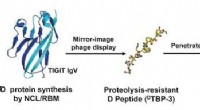
- Checkpointblokkade door een D-peptide voor kankerimmunotherapie
- Onderzoek onthult inzichten in enzym dat een algemeen broeikasgas bestrijdt

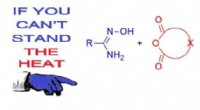
- Chemici ontwikkelen een veelbelovende methode voor medicijnsynthese
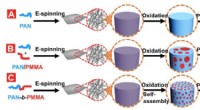
- Onderzoekers creëren eerste koolstofvezels met uniforme poreuze structuur
 Wat beschrijft genexpressie het beste het beste?
Wat beschrijft genexpressie het beste het beste?  Kunnen robots ons beschermen in de branding?
Kunnen robots ons beschermen in de branding? Argonchemie begrijpen:eigenschappen en reacties
Argonchemie begrijpen:eigenschappen en reacties  Nieuwe studie toont overdracht van epigenetisch geheugen over meerdere generaties
Nieuwe studie toont overdracht van epigenetisch geheugen over meerdere generaties Hoe de Wolbachia-bacterie vectoren van dodelijke ziekten controleert
Hoe de Wolbachia-bacterie vectoren van dodelijke ziekten controleert  Veelbelovende nieuwe legering voor resistief schakelgeheugen
Veelbelovende nieuwe legering voor resistief schakelgeheugen Hoe beleid te ontwerpen dat zowel de aquacultuur als de kleinschalige visserij ondersteunt
Hoe beleid te ontwerpen dat zowel de aquacultuur als de kleinschalige visserij ondersteunt  Wat is de definitie van AC -elektriciteit en DC -elektriciteit?
Wat is de definitie van AC -elektriciteit en DC -elektriciteit?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

