
Wetenschap
Ionische geleidbaarheid:waarom vaste stoffen geen elektriciteit geleiden - uitgelegd
* Solid State: In hun vaste toestand bestaan ionische verbindingen als een stijve roosterstructuur. De ionen worden stevig op vaste posities gehouden door sterke elektrostatische krachten. Deze krachten beperken de beweging van ionen, waardoor ze geen elektrische stroom kunnen dragen.
* Gesmolten of waterige toestand: Wanneer een ionische verbinding smelt of oplost in water, breken de ionen los van de roosterstructuur en worden ze mobiel. Deze mobiele ionen kunnen nu vrij bewegen en een elektrische stroom geleiden.
Hoe het werkt:
1. Elektrolyt: Wanneer een ionische verbinding in water wordt opgelost of gesmolten, vormt deze een elektrolyt . Dit betekent dat het vrij bewegende ionen bevat die elektriciteit kunnen geleiden.
2. Elektrisch veld: Wanneer een elektrisch veld over de elektrolyt wordt aangelegd, migreren de positieve ionen naar de negatieve elektrode (kathode) en de negatieve ionen naar de positieve elektrode (anode).
3. Elektrische stroom: Deze beweging van ionen creëert een elektrische stroom, waardoor de elektriciteit door de elektrolyt kan stromen.
Samengevat: Ionische verbindingen geleiden alleen elektriciteit als hun ionen vrij kunnen bewegen, wat gebeurt in gesmolten of opgeloste toestand. In hun vaste toestand voorkomen de vaste ionenposities geleidbaarheid.
 Hoe is Rust vorm?
Hoe is Rust vorm?  Wat worden als gunstige chemische reacties beschouwd?
Wat worden als gunstige chemische reacties beschouwd?  Onderzoekers ontdekken een nieuwe receptor die de functie van de voorlopercellen van de talgklier reguleert
Onderzoekers ontdekken een nieuwe receptor die de functie van de voorlopercellen van de talgklier reguleert Welke twee elementen zijn in natriumchloride?
Welke twee elementen zijn in natriumchloride?  Ontdekking verandert de manier waarop wetenschappers de zeldzaamste elementen van het periodiek systeem onderzoeken
Ontdekking verandert de manier waarop wetenschappers de zeldzaamste elementen van het periodiek systeem onderzoeken
Hoofdlijnen
- Waarom worden picogenen zo genoemd?
- Van welke vragen die leiden tot wetenschappelijke ontdekking worden geleverd?
- Wat is de functie van een prokatyotische cel?
- Wat is het proces dat verantwoordelijk is voor het verliezen van water in planten door transpiratie?
- Welke organel is verantwoordelijk voor CA -opslag in spiercellen?
- Welk lichaamssysteem verwijdert cellulaire en vloeistofafval?
- Wat is het type natuurlijke selectie dat tussenliggende fenotypes bevordert?
- Welk doel dient geheugen B en T -cellen te dienen?
- Hoe ziet een bacteriecel er anders uit dan de planten- en dierlijke cellen?
- Beheersing van ijsvorming op gradiëntbevochtigbare oppervlakken voor hoogwaardige bio-geïnspireerde materialen

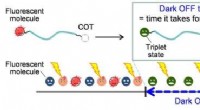
- Wanneer FRETing over kankerbiomarkers niet zal werken, focus in plaats daarvan op knipperen
- Hoe twee watermoleculen samen dansen

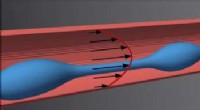
- Natuurkundigen ontdekken mechanisme voor vorming van bloedplaatjes
- Ook na handen wassen, nieuwe vingerafdruktest kan onderscheid maken tussen personen die heroïne hebben gebruikt of gebruikt

 Waar worden organische materialen gesynthetiseerd in planten?
Waar worden organische materialen gesynthetiseerd in planten?  Heeft de zon een as?
Heeft de zon een as?  "What is Pascals Triangle?
"What is Pascals Triangle? Bosbranden gekoppeld aan tienduizenden vermijdbare sterfgevallen
Bosbranden gekoppeld aan tienduizenden vermijdbare sterfgevallen Koralen in de Rode Zee bieden langetermijnzicht op de Zuid-Aziatische zomermoesson
Koralen in de Rode Zee bieden langetermijnzicht op de Zuid-Aziatische zomermoesson Instabiliteit in Antarctisch ijs zal naar verwachting de zeespiegel snel doen stijgen
Instabiliteit in Antarctisch ijs zal naar verwachting de zeespiegel snel doen stijgen Hoe vormt ammoniumion een onoplosbaar zout?
Hoe vormt ammoniumion een onoplosbaar zout?  Buisvormige zonnecellen kunnen in kleding worden geweven
Buisvormige zonnecellen kunnen in kleding worden geweven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

