
Wetenschap
Zuur-basereacties:pH-veranderingen begrijpen bij het mengen van zuren en basen
* Zuren hebben een lage pH (meestal lager dan 7), wat betekent dat ze een hoge concentratie waterstofionen (H+) hebben.
* Basisbasissen hebben een hoge pH (meestal boven 7), wat betekent dat ze een lage concentratie waterstofionen (H+) hebben.
Wanneer je een zuur en een base mengt, reageren de waterstofionen uit het zuur met de hydroxide-ionen (OH-) uit de base om water (H2O) te vormen. Deze reactie neutraliseert enkele zure en basische eigenschappen:
H+ + OH- → H2O
Naarmate de waterstofionen uit het zuur worden verbruikt, neemt de totale concentratie waterstofionen in de oplossing af. Omdat de pH een maatstaf is voor de waterstofionenconcentratie, neemt de pH van de oplossing af en komt dichter bij neutraal (pH 7).
Beschouw het als volgt:
* Je begint met een oplossing die veel "base" bevat (hoge pH).
* Het toevoegen van "zuur" is hetzelfde als het toevoegen van "zuur" om de "base" te neutraliseren.
* Hoe meer zuur je toevoegt, hoe minder "base" er is en hoe lager de pH wordt.
 Wat voor soort studies valt buiten de REAL -wetenschap?
Wat voor soort studies valt buiten de REAL -wetenschap?  Mariene diatomeeën vertonen een hoge plasticiteit bij het aanpassen aan fluctuerende lichtomstandigheden
Mariene diatomeeën vertonen een hoge plasticiteit bij het aanpassen aan fluctuerende lichtomstandigheden  Mexico's weg naar herstel na aardbevingen is veel langer dan het lijkt
Mexico's weg naar herstel na aardbevingen is veel langer dan het lijkt Wat betekent het respecteren van de omgeving?
Wat betekent het respecteren van de omgeving?  Wat beïnvloedt eigenlijk de luchtvervuiling boven de Indische Oceaan?
Wat beïnvloedt eigenlijk de luchtvervuiling boven de Indische Oceaan?
Hoofdlijnen
- Laat mijn brein me dingen kopen die ik niet nodig heb?
- Wat doet het Golgi -blaasjes ribosoom voor plantencel?
- Dragen plantencellen ademhaling en fotosynthese?
- Welke twee processen zijn betrokken bij seksuele reproductie?
- Wat is voorbeeld van chemosynthese?
- Watervlooien als kanaries in een kolenmijn bieden de sleutel tot het beheersen van chemische vervuiling
- Maakt het nucleolus deel van een dierlijke cel of plantencel?
- Segmenten van wat zijn overdracht van ouder tot nakomelingen genaamd genen?
- Wat is fylogenetische beperking?
- De reactiviteit van katalysatoren opsporen
- Om biologie te verbinden met elektronica, stijf zijn, maar toch flexibel
- Voor fotokatalysatoren, de tand des tijds doorstaan betekent een perfecte partner vinden

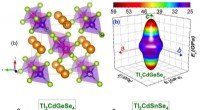
- Onderzoek naar nieuw gesynthetiseerde thalliumverbindingen voor opto-elektronische apparaten
- Is het hennep of marihuana? Nieuwe scanner geeft direct antwoord

 NASA's TESS-missie vindt zijn kleinste planeet tot nu toe
NASA's TESS-missie vindt zijn kleinste planeet tot nu toe Wat beschrijft het beste hoe stil en actieve zonneperioden verschillen?
Wat beschrijft het beste hoe stil en actieve zonneperioden verschillen?  Wordt MnSO4 ook wel Epsom-zout genoemd?
Wordt MnSO4 ook wel Epsom-zout genoemd?  Welk plateau in India is rijke minerale afzettingen?
Welk plateau in India is rijke minerale afzettingen?  Krachtige laserdiodes kunnen restspanning in 3D-geprinte metalen onderdelen verminderen
Krachtige laserdiodes kunnen restspanning in 3D-geprinte metalen onderdelen verminderen Wat heb je nodig om een objecten te weten snelheid?
Wat heb je nodig om een objecten te weten snelheid?  Wat zijn de stoffen die in water drijven?
Wat zijn de stoffen die in water drijven?  Welke dierengroepen hebben orgaansysteemniveau van organisatie?
Welke dierengroepen hebben orgaansysteemniveau van organisatie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

