
Wetenschap
Lewis-structuur van CHBr3 (Bromoform):een stapsgewijze handleiding
1. Valentie-elektronen tellen:
* Koolstof (C):4 valentie-elektronen
* Waterstof (H):1 valentie-elektron
* Broom (Br):elk 7 valentie-elektronen (3 broomatomen =21 elektronen)
Totale valentie-elektronen:4 + 1 + 21 =26
2. Centraal Atoom:
* Koolstof is het minst elektronegatieve element en zal dus het centrale atoom zijn.
3. Enkelvoudige obligaties:
* Verbind het centrale koolstofatoom met de waterstof- en drie broomatomen met enkele bindingen. Hierbij worden 8 elektronen gebruikt (4 bindingen x 2 elektronen/binding).
4. Resterende elektronen:
*Je hebt nog 18 elektronen over (26 - 8).
* Elk broomatoom heeft nog 6 elektronen nodig om zijn octet te voltooien (8 valentie-elektronen).
5. Compleet Octet:
* Plaats 3 vrije elektronenparen (elk 6 elektronen) rond elk broomatoom.
6. Lewis-structuur:
De uiteindelijke Lewis-structuur ziet er als volgt uit:
```
H
|
Br - C - Br
|
Br
```
Belangrijkste punten:
* Het koolstofatoom heeft een compleet octet met 4 bindingen.
* Elk broomatoom heeft een compleet octet met 1 binding en 3 alleenstaande paren.
* Het waterstofatoom heeft 2 elektronen (een compleet duet).
 Academische oproepen tot upgrade van rioleringssystemen om de gezondheid te beschermen
Academische oproepen tot upgrade van rioleringssystemen om de gezondheid te beschermen  Is maatschappelijke eisen vaak een drijvende kracht achter wetenschappelijk streven?
Is maatschappelijke eisen vaak een drijvende kracht achter wetenschappelijk streven?  Studie laat zien hoe permafrost methaan afgeeft in het opwarmende Noordpoolgebied
Studie laat zien hoe permafrost methaan afgeeft in het opwarmende Noordpoolgebied Natuurlijke oplossingen voor de klimaatcrisis? Een kwart bevindt zich helemaal op de aarde
Natuurlijke oplossingen voor de klimaatcrisis? Een kwart bevindt zich helemaal op de aarde  Uranium-immobiliserende bacteriën in kleigesteente:onderzoeken hoe micro-organismen het gedrag van radioactief afval kunnen beïnvloeden
Uranium-immobiliserende bacteriën in kleigesteente:onderzoeken hoe micro-organismen het gedrag van radioactief afval kunnen beïnvloeden
Hoofdlijnen
- Welke wetenschapper bestudeert abiotische factoren?
- Is eiwit een micro- of macro -molecuul?
- Leg uit hoe hypertoniciteit kan worden gebruikt als een middel om microbiële groei te beheersen?
- Wat is een dubbele ommuur met moleculen met hydrofobe staarten en hydrofiele kop die het in alle cellen heeft gevonden, wat regelt wat binnenkomt, verlaat de cel?
- Menselijk DNA wordt gesplitst in de?
- De impact van biotechnologie:het transformeren van individuen, de samenleving en het milieu
- Wat gebeurt er met een Zygote na de bevruchting?
- Hoeveel organismen moeten er in een voedselketen zijn om cellulaire ademhaling uit te voeren?
- Wat is de moleculaire structuur van een buitenaards wezen?
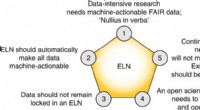
- Chemisch gegevensbeheer:een open weg voorwaarts
- Kooldioxide transformeren - onderzoekers ontwikkelen nieuwe tweestaps CO2-conversietechnologie

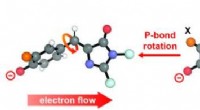
- Hoe elektrische velden een moleculaire draaiing in lichtgevoelige eiwitten beïnvloeden
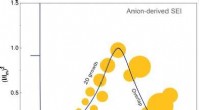
- Anionen en oplosmiddelen sturen kiemvorming en groei van de vaste elektrolyt-interfase
- Doorbraak metaalionen leidt tot nieuwe biomaterialen

 Welke kenmerken van de ster helpen ons te voorspellen hoe hij zich gaat gedragen?
Welke kenmerken van de ster helpen ons te voorspellen hoe hij zich gaat gedragen?  Gebruik van isolatoren en geleiders thuis?
Gebruik van isolatoren en geleiders thuis?  De bron van een autogene infectie is wat?
De bron van een autogene infectie is wat?  Welk subatomaire deeltje wordt gevonden in de kern van alle isotopen waterstof?
Welk subatomaire deeltje wordt gevonden in de kern van alle isotopen waterstof?  Wat is formule voor koperwaterstofsulfaat?
Wat is formule voor koperwaterstofsulfaat?  Wat is het witte poeder dat wordt gebruikt in Antacid?
Wat is het witte poeder dat wordt gebruikt in Antacid?  Hoe analyseert energie van de Sun Power Hurricanes?
Hoe analyseert energie van de Sun Power Hurricanes?  Hoeveel moleculen van koolmonoxide zijn deze verbinding in 3,69 gram aanwezig?
Hoeveel moleculen van koolmonoxide zijn deze verbinding in 3,69 gram aanwezig?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

