
Wetenschap
Lanthanide-elektronenconfiguratie:waarom 5d-elektronen eerst worden verwijderd
Belangrijkste concepten
* Energieniveau versus penetratie: Hoewel de 4f-orbitaal inderdaad een lagere energie heeft dan de 5d-orbitaal, is hij ook doordringender . Dit betekent dat 4f-elektronen meer tijd dichter bij de kern doorbrengen dan 5d-elektronen.
* Afscherming: De 4f-elektronen worden afgeschermd door de gevulde 5s- en 5p-orbitalen. Dit betekent dat de 4f-elektronen een zwakkere aantrekkingskracht op de kern ervaren vergeleken met 5d-elektronen.
* Effectieve nucleaire lading: Door afscherming ervaren 4f-elektronen een lagere effectieve nucleaire lading dan 5d-elektronen.
De uitleg
1. Lagere energie maar hogere penetratie: De 4f-orbitalen hebben een lagere energie, maar hebben een hogere penetratie vergeleken met 5d-orbitalen. Dit betekent dat 4f-elektronen steviger aan de kern zijn gebonden.
2. Afschermingseffect: De gevulde 5s- en 5p-orbitalen beschermen de 4f-elektronen tegen de kern, waardoor hun effectieve nucleaire lading wordt verminderd.
3. Eenvoudiger verwijderen: De 5d-elektronen, die door minder afscherming een sterkere effectieve nucleaire lading ervaren, worden minder stevig vastgehouden en zijn dus gemakkelijker te verwijderen.
In eenvoudiger bewoordingen:
Stel je voor dat de 4f-elektronen lijken op een groep mensen die dicht bij een kampvuur zitten, beschermd tegen de wind door een muur. De 5d-elektronen bevinden zich verder weg en worden blootgesteld aan de wind (wat de aantrekkingskracht van de kern vertegenwoordigt). Hoewel het kampvuur hetzelfde is (wat het energieniveau weergeeft), zijn de mensen die zich dichter bij het vuur bevinden (4f elektronen) beter beschermd en moeilijker te verplaatsen.
Gevolgen
Dit effect verklaart waarom lanthaniden de neiging hebben ionen te vormen met een lading van +3. Het verwijderen van elektronen uit de 5d-orbitaal leidt eerst tot een relatief stabiele configuratie, en verdere ionisatie wordt steeds moeilijker vanwege de stevig vastgehouden 4f-elektronen.
Belangrijke opmerking:
Hoewel deze verklaring over het algemeen juist is, is het belangrijk om te onthouden dat het feitelijke ionisatieproces complex is en door vele factoren wordt beïnvloed. Er zijn enkele uitzonderingen, en de volgorde van elektronenverwijdering is mogelijk niet altijd strikt 5d vóór 4f.
 Zal Alka-Seltzer sneller in tweeën oplossen?
Zal Alka-Seltzer sneller in tweeën oplossen?  Nieuwe test effent de weg voor mogelijke behandelingen om Alzheimer en andere aandoeningen aan te pakken
Nieuwe test effent de weg voor mogelijke behandelingen om Alzheimer en andere aandoeningen aan te pakken Gouden eiwitclusters kunnen worden gebruikt als milieu- en gezondheidsdetectoren
Gouden eiwitclusters kunnen worden gebruikt als milieu- en gezondheidsdetectoren Geologen en biologen ontdekken de atomaire vingerafdrukken van kanker
Geologen en biologen ontdekken de atomaire vingerafdrukken van kanker  Wat zijn de chemische reacties van de ozonlaag omdat mensen?
Wat zijn de chemische reacties van de ozonlaag omdat mensen?
 Betere afvalwaterzuivering? Het zit erop
Betere afvalwaterzuivering? Het zit erop Saoedi-Arabië wordt geconfronteerd met toenemende hitte, vochtigheid, extreme neerslag tegen het midden van de eeuw
Saoedi-Arabië wordt geconfronteerd met toenemende hitte, vochtigheid, extreme neerslag tegen het midden van de eeuw Uit onderzoek blijkt dat de stijging van de zeespiegel en weersgerelateerde schokken ervoor zorgden dat het moeras van Louisiana afstierf
Uit onderzoek blijkt dat de stijging van de zeespiegel en weersgerelateerde schokken ervoor zorgden dat het moeras van Louisiana afstierf  Sydney roept klimaatnoodtoestand uit - wat betekent dat in de praktijk?
Sydney roept klimaatnoodtoestand uit - wat betekent dat in de praktijk? Houden bomen werkelijk contact via een ‘houtbreed web’? Dit is wat het bewijsmateriaal zegt
Houden bomen werkelijk contact via een ‘houtbreed web’? Dit is wat het bewijsmateriaal zegt
Hoofdlijnen
- Onderzoek naar de genetica van macroalgen werpt licht op hoe zeewier meercellig werd
- Wat zijn de 5 wetenschappen die evolutie ondersteunen?
- Wat kan worden veroorzaakt door zuren geproduceerde plantenwortels?
- Bestaat er een wetenschappelijke formule voor grappig?
- Wat doet SDS met cellen?
- Hoe zijn computervirussen vergelijkbaar met en verschillend van biologische virussen?
- Welke cellen in het lichaam worden gedeeld door meiose?
- Studie onthult hoe DNA zich ontvouwt voor transcriptie
- Cellen van een organisme voeren de volgende chemische reactie 6 CO2 plus H2O en Rarr C6H12O6 O2 uit welke deze cellen waarschijnlijk behoren?
- CO2-neutrale waterstof uit biomassa

- Converteer normaliteit naar grammen:stapsgewijze handleiding voor nauwkeurige berekeningen

- Nog een reden om van de gestreepte bas te houden:antimicrobiële middelen

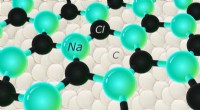
- De moeite waard:onderzoekers melden eerste geval van hexagonaal NaCl
- Wetenschappers ontwikkelen sondes die zijn ontworpen om de fysieke krachten in levende cellen te onthullen; een wereldprimeur

 Wat zijn niet-de-ziekte-producerende micro-organismen?
Wat zijn niet-de-ziekte-producerende micro-organismen?  Hoe kan de index van brekingszoutwater worden gebruikt om een concentratieoplossing te vinden?
Hoe kan de index van brekingszoutwater worden gebruikt om een concentratieoplossing te vinden?  Wat is waterdamp die is gecondenseerd?
Wat is waterdamp die is gecondenseerd?  Eenvoudige arseensensor kan levens redden
Eenvoudige arseensensor kan levens redden Was Tricia de olifant blij? Deskundigen bespreken de ethiek van het in gevangenschap houden van zulke grote, rondzwervende wezens
Was Tricia de olifant blij? Deskundigen bespreken de ethiek van het in gevangenschap houden van zulke grote, rondzwervende wezens  Welke twee terrestrische planeten hebben de meest vergelijkbare atmosferische samenstelling?
Welke twee terrestrische planeten hebben de meest vergelijkbare atmosferische samenstelling?  Wat de AT&T-T-Mobile-deal voor klanten zou kunnen betekenen
Wat de AT&T-T-Mobile-deal voor klanten zou kunnen betekenen  De ë v is hetzelfde als het eindigen van snelheid wanneer het object begint?
De ë v is hetzelfde als het eindigen van snelheid wanneer het object begint?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

