
Wetenschap
Inzicht in de OH-concentratie in zwavelzuuroplossingen
Hier leest u hoe u de OH⁻-concentratie in een zwavelzuuroplossing kunt begrijpen:
* Eerste ionisatie: H₂SO₄ ioniseert volledig in water en doneert één proton om HSO₄⁻ (waterstofsulfaation) en H₃O⁺ (hydroniumion) te vormen.
* H₂SO₄ (aq) + H₂O (l) → HSO₄⁻ (aq) + H₃O⁺ (aq)
* Tweede ionisatie: HSO₄⁻ ioniseert ook, maar in mindere mate, en doneert nog een proton om SO₄²⁻ (sulfaation) en nog een H₃O⁺ te vormen.
* HSO₄⁻ (aq) + H₂O (l) ⇌ SO₄²⁻ (aq) + H₃O⁺ (aq)
De hoge concentratie H₃O⁺-ionen verlaagt de OH⁻-concentratie aanzienlijk vanwege de ionenproductconstante van water (Kw):
* Kw =[H₃O⁺][OH⁻] =1,0 × 10⁻¹⁴ bij 25°C
Daarom is de OH⁻-concentratie in een zwavelzuuroplossing extreem laag. Om de exacte waarde te berekenen, moet u de concentratie van de zwavelzuuroplossing kennen en beide ionisatiestappen overwegen.
Belangrijkste punten:
* Zwavelzuur is een sterk zuur, wat betekent dat het in oplossing volledig ioniseert.
*De aanwezigheid van H₃O⁺-ionen uit het zuur verlaagt de OH⁻-concentratie aanzienlijk.
*De exacte OH⁻-concentratie is afhankelijk van de concentratie van de zwavelzuuroplossing.
 Wat gebeurt er met de elektronentransportketen als er geen zuurstof is?
Wat gebeurt er met de elektronentransportketen als er geen zuurstof is?  Zal zout water koken of kookt regelmatig?
Zal zout water koken of kookt regelmatig?  Onderzoek identificeert een chemisch mechanisme dat laat zien hoe ijzer in de bodem arseen kan immobiliseren
Onderzoek identificeert een chemisch mechanisme dat laat zien hoe ijzer in de bodem arseen kan immobiliseren  Hoe kunt u de kristallisatie uitleggen met behulp van de deeltjestheorie?
Hoe kunt u de kristallisatie uitleggen met behulp van de deeltjestheorie?  Het atmosferische gas dat een mild zuur vormt wanneer opgelost in water is?
Het atmosferische gas dat een mild zuur vormt wanneer opgelost in water is?
 Onderzoekers ontdekken dat landschapsruggen aanwijzingen kunnen bevatten over ijstijd en klimaatverandering
Onderzoekers ontdekken dat landschapsruggen aanwijzingen kunnen bevatten over ijstijd en klimaatverandering Nieuwe 3D-beeldtechnologie brengt Schotse koraalriffen in kaart
Nieuwe 3D-beeldtechnologie brengt Schotse koraalriffen in kaart Satellieten combineren, radar biedt pad voor betere voorspellingen
Satellieten combineren, radar biedt pad voor betere voorspellingen Hoe beïnvloedt kunst de wetenschap?
Hoe beïnvloedt kunst de wetenschap?  Het beschermen van tropische bossen heeft een bijkomend voordeel:het vertragen van de klimaatverandering
Het beschermen van tropische bossen heeft een bijkomend voordeel:het vertragen van de klimaatverandering
Hoofdlijnen
- Een viraal verhulapparaat:Biologen laten zien hoe het menselijke cytomegalovirus zich verbergt voor het immuunsysteem
- Wat is polygene erfenis?
- Wat is het doel van fruitvlieglab?
- Waarom is het onwaarschijnlijk dat plasmolyse in de natuur opkomt?
- Hoe heet een geprogrammeerde cel?
- Wat zijn stamcellen en waarvoor worden ze gebruikt?
- Wat is de wetenschappelijke notatie van een bij?
- Waarom geven we de voorkeur aan bepaalde voedingsmiddelen boven andere?
- Anti-verouderingsbehandelingen - de wetenschap van het leven langer
- Onderzoekers ontwikkelen katalysator met chiraliteit in het zinkcentrum
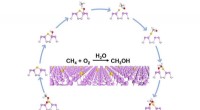
- Goud-fosfor-nanobladen katalyseren selectief aardgas tot groenere energie
- Interactieve kaart van metabolische synthese van chemicaliën

- Welk gas zorgt voor de paarse gloed in neonreclame?

- Niet-kloneerbare tag bestrijdt vervalsers

 Verspreiden bacteriën en virus zich op dezelfde manier?
Verspreiden bacteriën en virus zich op dezelfde manier?  270 kg is hoeveel pond?
270 kg is hoeveel pond?  Uber treedt op tegen LHBT-discriminatie tijdens Nederlandse gay pride
Uber treedt op tegen LHBT-discriminatie tijdens Nederlandse gay pride Wat vormt als het landblok tussen twee normale fouten naar beneden glijdt?
Wat vormt als het landblok tussen twee normale fouten naar beneden glijdt?  Waarom als je naar een rots onder water kijkt, lijkt het zich in een andere positie te bevinden?
Waarom als je naar een rots onder water kijkt, lijkt het zich in een andere positie te bevinden?  Hoe u een berengewicht meet aan de voetmaat
Hoe u een berengewicht meet aan de voetmaat Waarom wordt het water als materie beschouwd?
Waarom wordt het water als materie beschouwd?  Nieuwe nanokristallen tonen potentieel voor goedkope lasers en nieuwe verlichting
Nieuwe nanokristallen tonen potentieel voor goedkope lasers en nieuwe verlichting
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

