
Wetenschap
Verdamping begrijpen:hoe vloeistoffen in gas worden omgezet
1. Warmte-energie: De sleutel is het toevoegen van warmte-energie aan de vloeistof. Deze energie zorgt ervoor dat de moleculen in de vloeistof sneller en verder uit elkaar bewegen.
2. Intermoleculaire krachten overwinnen: Vloeistoffen worden bij elkaar gehouden door zwakke intermoleculaire krachten (zoals waterstofbruggen, van der Waals-krachten). Naarmate de moleculen energie winnen, trillen ze krachtiger, overwinnen ze deze krachten en breken ze los van het vloeistofoppervlak.
3. Verandering van staat: Zodra de moleculen voldoende energie hebben, ontsnappen ze aan het vloeistofoppervlak en komen in de gasvormige toestand terecht.
Twee belangrijke soorten vaporisatie:
* Verdamping: Dit is een geleidelijk proces dat bij elke temperatuur aan het oppervlak van een vloeistof plaatsvindt. Moleculen met een hogere kinetische energie ontsnappen uit de vloeistof en worden damp. Daarom drogen plassen uiteindelijk op, zelfs op koele dagen.
* Koken: Dit gebeurt wanneer de vloeistof het kookpunt bereikt, de temperatuur waarbij de dampdruk van de vloeistof gelijk is aan de druk eromheen. De vloeistof verandert vervolgens in het hele volume in een gas, niet alleen aan het oppervlak.
Factoren die de verdamping beïnvloeden:
* Temperatuur: Hogere temperaturen leiden tot snellere verdamping.
* Oppervlakte: Grotere oppervlakken zorgen ervoor dat meer moleculen in de gasfase kunnen ontsnappen.
* Atmosferische druk: Een lagere atmosferische druk maakt het gemakkelijker voor moleculen om naar de gasfase te ontsnappen.
Samenvattend verandert vloeistof in gas wanneer de moleculen voldoende energie verkrijgen om de krachten te overwinnen die ze in vloeibare toestand bij elkaar houden. Dit proces wordt verdamping genoemd en kan geleidelijk (verdamping) of snel (koken) plaatsvinden.
 'Eén ring om ze allemaal te regeren':hoe actinefilamenten worden samengesteld door formines
'Eén ring om ze allemaal te regeren':hoe actinefilamenten worden samengesteld door formines  Wat is het percentage concentratie van chloor in natriumchloride?
Wat is het percentage concentratie van chloor in natriumchloride?  Wat beschrijft elementen die worden gemaakt in deeltjesversnellers en niet de natuur gevonden?
Wat beschrijft elementen die worden gemaakt in deeltjesversnellers en niet de natuur gevonden?  Urinekristallen:identificatie en betekenis
Urinekristallen:identificatie en betekenis  Zijn de meeste chemische reacties in levende cellen in evenwicht?
Zijn de meeste chemische reacties in levende cellen in evenwicht?
 Studie vindt natuurbrandgevaar in woonhekken en mulchbedden
Studie vindt natuurbrandgevaar in woonhekken en mulchbedden Waarom smaakt wat kraanwater raar?
Waarom smaakt wat kraanwater raar? Welke vegetatie is er in de Tierra Templada?
Welke vegetatie is er in de Tierra Templada?  Zuid-Afrika om kolengestookte energie te verhogen, klimaatverontwaardiging aanwakkeren
Zuid-Afrika om kolengestookte energie te verhogen, klimaatverontwaardiging aanwakkeren Watergebruik in de VS daalt tot niveaus die sinds 1970 niet meer zijn gezien
Watergebruik in de VS daalt tot niveaus die sinds 1970 niet meer zijn gezien
Hoofdlijnen
- Wat is de celstructuur van Rhizopus stolonifer?
- Waarom vriezen vissen niet dood in ijskoud water?
- Ware of valse cellen groeperen samen om organen te vormen en weefsel te combineren?
- Een diagram dat waarschijnlijke evolutionaire relaties tussen oraganisme vertoont, wordt een genoemd?
- Is het waar of onwaar dat chromosomen die genen dragen worden gevonden in de kern van cel?
- Wat wordt bedoeld met homozygenous?
- Wat is de enige functie van eiwitten in een cel?
- Wat is de epidermale cel die een rol speelt in immuniteit en ziektebestendigheid?
- Wat bestaat uit genen?
- Algen als microscopisch kleine bioraffinaderijen
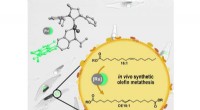
- Nieuw proces versnelt medicamenteuze behandelingen voor virale infecties en kanker

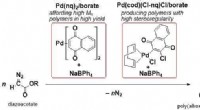
- Nieuwe op palladium gebaseerde initiatiesystemen voor C1-polymerisatie van diazoacetaten
- Een demonstratie van real-space beeldvorming van enkele van de meest representatieve vormen van gehydrateerde protonen

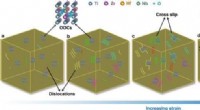
- Verbeterde sterkte en taaiheid in een legering met hoge entropie via geordende zuurstofcomplexen
 Wat zijn alluviale terrassen?
Wat zijn alluviale terrassen?  Hoe zien we niet-lichtgevende objecten?
Hoe zien we niet-lichtgevende objecten?  Chemische versus fysische eigenschappen:dichtheid begrijpen
Chemische versus fysische eigenschappen:dichtheid begrijpen  Hoe celorganellen samenwerken
Hoe celorganellen samenwerken  Welk gas is meer ideaal N2 of HBR en waarom?
Welk gas is meer ideaal N2 of HBR en waarom?  Wat is de nuttige en verspilde energie in een föhn?
Wat is de nuttige en verspilde energie in een föhn?  Nieuwe techniek controleert de afmetingen van gouden nanostaafjes tijdens de productie op grote schaal
Nieuwe techniek controleert de afmetingen van gouden nanostaafjes tijdens de productie op grote schaal Wie observeerde voor het eerst de fusie van lichte kernen en in welk jaar?
Wie observeerde voor het eerst de fusie van lichte kernen en in welk jaar?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

