
Wetenschap
Meest reactieve metalen:alkalische en alkalische aardefamilies uitgelegd
De twee families in het periodiek systeem met de meest reactieve metalen zijn:
* Alkalimetalen (Groep 1): Deze metalen hebben slechts één valentie-elektron, waardoor ze heel graag dit willen verliezen en een +1-ion willen vormen. Dit maakt ze extreem reactief, vooral met water. Voorbeelden zijn onder meer lithium (Li), natrium (Na), kalium (K), rubidium (Rb), cesium (Cs) en frankium (Fr).
* Aardalkalimetalen (Groep 2): Deze metalen hebben twee valentie-elektronen, die ze gemakkelijk verliezen om +2 ionen te vormen. Ze zijn minder reactief dan alkalimetalen, maar nog steeds zeer reactief. Voorbeelden zijn onder meer beryllium (Be), magnesium (Mg), calcium (Ca), strontium (Sr), barium (Ba) en radium (Ra).
 Lichtpuntje tijdens COVID-19:Meer vermogen zonnepanelen dankzij schonere lucht
Lichtpuntje tijdens COVID-19:Meer vermogen zonnepanelen dankzij schonere lucht Waarom is het nauwkeuriger om de biosfeer te definiëren als een wereldwijd ecosysteem in plaats van gemeenschap?
Waarom is het nauwkeuriger om de biosfeer te definiëren als een wereldwijd ecosysteem in plaats van gemeenschap?  Dodelijke hittegolven zullen gebruikelijk zijn in Zuid-Azië, zelfs bij 1,5 graad opwarming
Dodelijke hittegolven zullen gebruikelijk zijn in Zuid-Azië, zelfs bij 1,5 graad opwarming Spuitbussen hebben invloed op de opbrengst van zonne-energie in Europa
Spuitbussen hebben invloed op de opbrengst van zonne-energie in Europa Hitte verdrijft wolken die bosbranden in Californië dempen
Hitte verdrijft wolken die bosbranden in Californië dempen
Hoofdlijnen
- Welke twee moleculen combineren om ATP te vormen?
- Studie wakkert de discussie aan over waarom vrouwtjesvogels extra partners zoeken
- Wie tweet er over wetenschappelijk onderzoek? En waarom?
- Hoe enzymen werken:UB-chemici publiceren een belangrijke ontdekking
- Cellulaire organisatie:het menselijke spijsverteringssysteem uitgelegd
- Hoe zorgen planten voor hun zaden?
- Wat?
- Wat wordt er geconsumeerd tijdens het proces van cellulaire ademhaling?
- Eerste stappen om de biochemie te begrijpen van hoe planten geuren detecteren
- Nieuwe katalysator met dubbele functie voor waterstof- en plasticproductie

- Stijve, pijnlijke knieën? In het laboratorium gemaakte kraakbeengel presteert beter dan het echte werk

- Schimmelverbinding remt belangrijke groep eiwitten

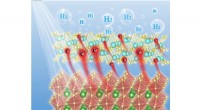
- Het maken van waterstof versnellen met een niet-edele metalen cokatalysator onder zichtbaar licht
- Nieuw licht op het maken van tweedimensionale polymeren

 Bevat een exotherme reactie meer chemische energie dan reactanten?
Bevat een exotherme reactie meer chemische energie dan reactanten?  Google zegt dat partner geheime Nederlandse gegevens heeft gelekt
Google zegt dat partner geheime Nederlandse gegevens heeft gelekt Indias Chandrayaan 2 maakt de kaart met de hoogste resolutie die we van de maan hebben
Indias Chandrayaan 2 maakt de kaart met de hoogste resolutie die we van de maan hebben Waarom zie je het noorderlicht alleen op bepaalde plaatsen?
Waarom zie je het noorderlicht alleen op bepaalde plaatsen?  Het tijdperk van single-spin kleurcentra in siliciumcarbide nadert
Het tijdperk van single-spin kleurcentra in siliciumcarbide nadert Wat is Flea Ecto Parasite?
Wat is Flea Ecto Parasite?  Dat beschrijft de relatie tussen potentiële en kinetische energie wanneer een pool zijn maximale buigpunt heeft bereikt?
Dat beschrijft de relatie tussen potentiële en kinetische energie wanneer een pool zijn maximale buigpunt heeft bereikt?  Wanneer een amplitude toeneemt, verandert de frequentie?
Wanneer een amplitude toeneemt, verandert de frequentie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

