
Wetenschap
De ruimte tussen atomen en moleculen begrijpen:elektronenwolken uitgelegd
Hier is een overzicht:
* Atomen bestaan uit een kern (die protonen en neutronen bevat) omgeven door een wolk van negatief geladen elektronen.
* Moleculen worden gevormd wanneer twee of meer atomen aan elkaar binden. Deze bindingen worden gevormd door het delen of overbrengen van elektronen tussen de atomen.
De ruimte tussen atomen en moleculen is gevuld met het volgende:
* Elektronenwolken: De elektronen rondom de atomen zijn voortdurend in beweging en creëren een diffuse wolk van negatieve lading. Deze wolk is verantwoordelijk voor de interacties tussen atomen en moleculen, inclusief chemische bindingen.
* Elektromagnetische velden: De beweging van elektronen creëert elektromagnetische velden die zich uitstrekken tot in de ruimte tussen atomen en moleculen. Deze velden spelen een rol bij het bepalen van de sterkte en het type interacties tussen moleculen.
* Lege ruimte: Hoewel de ruimte tussen atomen en moleculen niet helemaal leeg is, bevat deze wel een aanzienlijke hoeveelheid ‘lege’ ruimte vergeleken met het volume dat door de atomen zelf wordt ingenomen.
Belangrijke punten om te onthouden:
* De elektronen in de ruimte tussen de atomen zijn niet stationair, ze zijn voortdurend in beweging en interageren met elkaar.
* De rangschikking van deze elektronen en de sterkte van hun interacties bepalen de eigenschappen van de stof, zoals het smeltpunt, kookpunt en reactiviteit.
* De ‘lege’ ruimte tussen atomen en moleculen is niet echt leeg, maar eerder gevuld met de energie en velden die met de elektronen samenhangen.
Het begrijpen van de aard van de ruimte tussen atomen en moleculen is cruciaal voor het begrijpen van de eigenschappen en het gedrag van materie op atomair en moleculair niveau.
 Hoe de Lattice-energie van een verbinding te vinden
Hoe de Lattice-energie van een verbinding te vinden  Wat is een generieke naam voor de subatomaire deeltjes in kern van een atoom?
Wat is een generieke naam voor de subatomaire deeltjes in kern van een atoom?  Is zuur een natuurlijk gemaakte vaste stof met regelmatige opstelling van deeltjes erin?
Is zuur een natuurlijk gemaakte vaste stof met regelmatige opstelling van deeltjes erin?  Wat absorbeert koolstofdioxide uit de atmosfeer?
Wat absorbeert koolstofdioxide uit de atmosfeer?  Gastuitlijning en defectvorming tijdens porievulling in metaal-organische raamwerkfilms
Gastuitlijning en defectvorming tijdens porievulling in metaal-organische raamwerkfilms
 Waarom mensen in rampgevoelige steden blijven
Waarom mensen in rampgevoelige steden blijven Hoe heet waren de oceanen toen het leven zich voor het eerst ontwikkelde?
Hoe heet waren de oceanen toen het leven zich voor het eerst ontwikkelde? Voor Ghana recyclers van e-waste, een veiligere optie te midden van giftige dampen
Voor Ghana recyclers van e-waste, een veiligere optie te midden van giftige dampen Versnelde uitspoeling van radiocesium uit strooisel op de bosbodem door hevige regenval
Versnelde uitspoeling van radiocesium uit strooisel op de bosbodem door hevige regenval 4 redenen waarom een door gas geleid economisch herstel verschrikkelijk is, naïef idee
4 redenen waarom een door gas geleid economisch herstel verschrikkelijk is, naïef idee
Hoofdlijnen
- Hoe verschillen dierlijke cellen van plantencellen?
- Wat heeft Eukaryote die Prokayote niet?
- Wat is verantwoordelijk voor het dragen van u berichten van DNA in de kern in cytoplasma?
- Wat is een kenmerk van wei-eiwit?
- Het proces welke cellen uniquie -kenmerken ontwikkelen in structuur en functie wordt opgeroepen?
- Welke term betekent letterlijk vergelijking van vorm of vorm en omvat het anatomie -ontwikkelingsorganisme?
- Hoe lang duurt het voordat zwarte schimmel je doodt?
- Welke soorten kenmerken gebruiken wetenschappers om levende wezens te classificeren?
- Eiwitsynthese op de oorspronkelijke aarde kan zijn gekatalyseerd door --- vóór evolutie van enzymen?
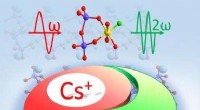
- Onderzoek onthult het eerste niet-centrosymmetrische fluoroxosilicofosfaat met Si-F-bindingen
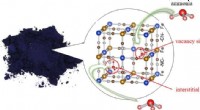
- Een blauw pigment dat een hoogwaardig ammoniakadsorbens blijkt te zijn
- Nieuwe toedieningsmethode maakt langzame afgifte van een breder scala aan peptidegeneesmiddelen in het lichaam mogelijk

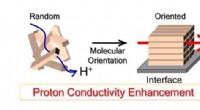
- Meer controle krijgen over brandstofcelmembranen
- Team ontdekt dubbele helixstructuur in synthetisch macromolecuul

 Een roestige groene vroege oceaan? Lab herschept één mechanisme waarmee de huidige ertsafzettingen oorspronkelijk werden gevormd
Een roestige groene vroege oceaan? Lab herschept één mechanisme waarmee de huidige ertsafzettingen oorspronkelijk werden gevormd Na 1984:nauwe focus op natuurbrandtrends onderschat toekomstige risico's voor waterveiligheid
Na 1984:nauwe focus op natuurbrandtrends onderschat toekomstige risico's voor waterveiligheid Het voordeel van het hebben van veel replicatie-origines in een eukaryotisch chromosoom
Het voordeel van het hebben van veel replicatie-origines in een eukaryotisch chromosoom Voorlader specificaties
Voorlader specificaties  Wanneer is Half Moon -onderzoeken gecreëerd?
Wanneer is Half Moon -onderzoeken gecreëerd?  Wat is de juiste volgorde tijdens een maansverduistering?
Wat is de juiste volgorde tijdens een maansverduistering?  Wat zijn de drie hoofdrollen die worden gespeeld door bacteriën in de stikstofcyclus?
Wat zijn de drie hoofdrollen die worden gespeeld door bacteriën in de stikstofcyclus?  Hoeveel millimeters zijn er in gallon?
Hoeveel millimeters zijn er in gallon?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

