
Wetenschap
Waterstofbinding:ionische en covalente interacties uitgelegd
Hier is een overzicht:
Ionische binding:
* Waterstof vormt doorgaans ionische bindingen met zeer elektronegatieve elementen zoals halogenen (F, Cl, Br, I), zuurstof (O) en stikstof (N) .
* In deze bindingen verliest waterstof zijn enkele elektron en vormt een positief geladen waterstofion (H+) . Dit ion trekt vervolgens de negatief geladen ionen van het andere element aan.
Covalente binding:
* Waterstof vormt covalente bindingen met elementen die vergelijkbare elektronegativiteitswaarden hebben, zoals koolstof (C), fosfor (P), zwavel (S) en andere waterstofatomen .
* Bij covalente bindingen deelt waterstof zijn enkele elektron met het andere element, waardoor een gedeeld elektronenpaar ontstaat. Dit gedeelde paar wordt aangetrokken door de kernen van beide atomen en houdt ze bij elkaar.
Voorbeelden van waterstofbinding:
* Water (H2O): Waterstof vormt covalente bindingen met zuurstof.
* Methaan (CH4): Waterstof vormt covalente bindingen met koolstof.
* Zoutzuur (HCl): Waterstof vormt een ionische binding met chloor.
* Ammoniak (NH3): Waterstof vormt covalente bindingen met stikstof.
Belangrijke opmerking: Waterstof kan ook metaalbindingen vormen in sommige metaalhydriden.
Belangrijkste punt: Het type binding dat wordt gevormd tussen waterstof en een ander element hangt af van het verschil in hun elektronegativiteit.
 Het bouwen van een betere brandstofcel begint met oppervlaktechemie
Het bouwen van een betere brandstofcel begint met oppervlaktechemie Welke van deze is een voorbeeld een samengesteld ijzer- of koolstofdioxide -zuurstofcalcium?
Welke van deze is een voorbeeld een samengesteld ijzer- of koolstofdioxide -zuurstofcalcium?  Wat zijn de waarnemingen als je ammoniummetavanadaat verwarmt in een nikkelkroes?
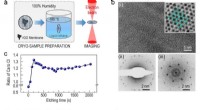
Wat zijn de waarnemingen als je ammoniummetavanadaat verwarmt in een nikkelkroes?  Nucleatiekinetiek in kaart brengen met nanometerresolutie
Nucleatiekinetiek in kaart brengen met nanometerresolutie Wat zijn het gemeenschappelijke laboratoriumapparaat en wat 30 en gebruikt?
Wat zijn het gemeenschappelijke laboratoriumapparaat en wat 30 en gebruikt?
 Lood terugwinnen, plastic, en zwavelzuur uit gebruikte autobatterijen
Lood terugwinnen, plastic, en zwavelzuur uit gebruikte autobatterijen Nieuwe drone-technologie verbetert het vermogen om vulkaanuitbarstingen te voorspellen
Nieuwe drone-technologie verbetert het vermogen om vulkaanuitbarstingen te voorspellen Southampton naar Shanghai met de trein:een zoektocht van onderzoekers naar klimaatverandering om vliegen te vermijden
Southampton naar Shanghai met de trein:een zoektocht van onderzoekers naar klimaatverandering om vliegen te vermijden De logica van bescheidenheid:waarom het loont om nederig te zijn
De logica van bescheidenheid:waarom het loont om nederig te zijn  NASA vindt windschering die Lowells sterkste stormen verdringt
NASA vindt windschering die Lowells sterkste stormen verdringt
Hoofdlijnen
- Wat zou er gebeuren als alle mitochondriën tijdens de mitose slechts in één cel zouden gaan?
- Het is misschien tijd om de houdbaarheidsdatum op voedselverpakkingen te schrappen, zeggen slimme verpakkingsonderzoekers
- Wat is epigenetica en waarom het belangrijk is?
- De positieve kant van een besmettelijk eiwit:stresssensoren bevorderen de overleving van gistcellen
- Cellen gebruiken het proces van mitose om te delen tijdens aseksuele reproductie?
- Maken dier eukaryote cellen suiker?
- Wat bevatten cellen geproduceerd in mitose?
- Welke van deze structuren is uniek voor plantencellen?
- Hoe reproduceren de meeste schimmels?
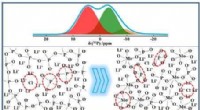
- Nieuw waargenomen eenwaardige calciumionen vertonen onverwachte metaalachtigheid en ferromagnetisme
- Georganiseerde chaos in het enzymcomplex - verrassende inzichten en nieuwe perspectieven

- Enkele atomen verbreken de sterkste binding van koolstof

- Onderzoekers onderzoeken de structuur van fosfaationische geleidende glazen met behulp van vastestof NMR
- Organische 2-oxocarbonzuren zorgen voor een link naar de vorming van radicalen en reactieve zuurstofsoorten in atmosferische deeltjes
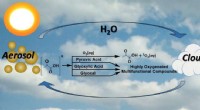
 Hoe zijn bergen en heuvels hetzelfde?
Hoe zijn bergen en heuvels hetzelfde?  Wat is het BHOR -diagram van chloor?
Wat is het BHOR -diagram van chloor?  Nieuwe anisotrope geleidende film voor montagetoepassingen met ultrafijne pitch
Nieuwe anisotrope geleidende film voor montagetoepassingen met ultrafijne pitch Hoe label je momenteel de lagen Mount St Helens?
Hoe label je momenteel de lagen Mount St Helens?  Beschrijf de noordelijke locatie op aarde.?
Beschrijf de noordelijke locatie op aarde.?  Regent het ooit echt uit de lucht?
Regent het ooit echt uit de lucht?  Een gemeenschappelijk energieknooppunt
Een gemeenschappelijk energieknooppunt Waarom is convectie belangrijker dan geleiding in de troposfeer?
Waarom is convectie belangrijker dan geleiding in de troposfeer?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

