
Wetenschap
Wat is het BHOR -diagram van chloor?
Inzicht in het Bohr -model
Het Bohr -model is een vereenvoudigde manier om de opstelling van elektronen in een atoom te visualiseren. Het geeft weer:
* Nucleus: Het midden van het atoom dat protonen en neutronen bevat.
* elektronenschalen: Cirkelvormige banen rond de kern waar elektronen verblijven. Elke schaal heeft een specifiek energieniveau.
* elektronen: Kleine deeltjes met een negatieve lading die de schelpen bezetten.
het creëren van het chloorbohr -diagram
1. Identificeer het atoomnummer: Chloor heeft een atoomnummer van 17. Dit betekent dat het 17 protonen en 17 elektronen heeft.
2. Teken de kern: Teken in het midden een cirkel die de kern vertegenwoordigt. Schrijf in de cirkel "17p+" om de 17 protonen aan te geven. U kunt ook het aantal neutronen opnemen (dat 18 is voor de meest voorkomende isotoop van chloor), maar dit wordt niet altijd weergegeven in een basis BOHR -diagram.
3. Elektronenschalen: Teken concentrische cirkels (of ringen) rond de kern om de elektronenschalen weer te geven. Chloor heeft drie elektronenschalen.
4. Elektronenplaatsing:
* De eerste schaal (het dichtst bij de kern) Kan maximaal 2 elektronen bevatten. Vul het met twee elektronen.
* De tweede shell Kan maximaal 8 elektronen bevatten. Vul het met 8 elektronen.
* De derde shell heeft de resterende 7 elektronen.
Het laatste diagram
Uw chloorbohr -diagram zou er zo uit moeten zien:
`` `
2e-
/ \
8e- 7e-
\ _____/
17p+
`` `
Sleutelpunten:
* De elektronen in de buitenste schaal (de valentie -elektronen) bepalen het chemische gedrag van het atoom. Chloor heeft 7 valentie -elektronen, waardoor het zeer reactief is.
* Het Bohr -model is een nuttig visueel hulpmiddel, maar is geen perfecte weergave van de atomaire structuur. Moderne modellen, zoals het kwantummechanische model, bieden een nauwkeuriger beeld.
 Klimaatgedreven evolutie in bomen verandert hun ecosystemen
Klimaatgedreven evolutie in bomen verandert hun ecosystemen Een stad definiëren met behulp van mobiele telefoongegevens
Een stad definiëren met behulp van mobiele telefoongegevens  2020 evenaart 2016 als warmste jaar ooit
2020 evenaart 2016 als warmste jaar ooit Onderzoek laat zien hoe planten beslissen tussen leven en dood
Onderzoek laat zien hoe planten beslissen tussen leven en dood  Duitsers zijn voorstander van een snelle stopzetting van het gebruik van steenkool naarmate het besluit nadert
Duitsers zijn voorstander van een snelle stopzetting van het gebruik van steenkool naarmate het besluit nadert
Hoofdlijnen
- Hoe damselfish en myside garnalen naast elkaar bestaan in een wederzijds voordelige relatie
- Microben reizen door de lucht; Het zou goed zijn om te weten hoe en waar
- Wat is het basisidee van theïstische evolutie?
- Wat wordt kraakbeen geproduceerd door?
- Wat is het bouwproces van lipiden?
- Waarom hebben cellen verschillende vormen en uiterlijk?
- Wetenschappers ontdekken waarom rijp fruit gevoeliger is voor necrotrofe ziekteverwekkers dan onrijp fruit
- Wat is synaptische varicositeit die verwijst naar hoe veranderingen in sensibilisatie van Aplysia?
- Typen morfologie
- Organische elektronica:een nieuwe halfgeleider in de koolstofnitride-familie

- Voordelige papieren sensor identificeert nauwkeurig pathogene bacteriën

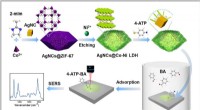
- Nieuwe SERS-sensor helpt bij het detecteren van aldehydegassen
- Nieuwe chemische methode vereenvoudigt modificatie in een laat stadium van medicijnverbindingen

- Doorbraak in het begrijpen van enzymen die antibiotica maken voor resistente ziekteverwekkers

 Onderzoekers komen soms dingen tegen waar ze niet naar op zoek zijn
Onderzoekers komen soms dingen tegen waar ze niet naar op zoek zijn  Samsung zegt dat het gegevens heeft gelekt over een handvol Britse klanten
Samsung zegt dat het gegevens heeft gelekt over een handvol Britse klanten Ghosn moet voor de rechter verschijnen:wat gebeurt er daarna?
Ghosn moet voor de rechter verschijnen:wat gebeurt er daarna? Wat zijn de basisconcepten van de wetenschap?
Wat zijn de basisconcepten van de wetenschap?  Wat is het abstracte zelfstandig naamwoord voor intuïtief?
Wat is het abstracte zelfstandig naamwoord voor intuïtief?  Siliciumsandwiches voeden LHC's opgewaardeerde botsingslust
Siliciumsandwiches voeden LHC's opgewaardeerde botsingslust Wat is de introductie van chemische fysische of biologische middelen in water die afgebroken is?
Wat is de introductie van chemische fysische of biologische middelen in water die afgebroken is?  Hoe krijgt water energie?
Hoe krijgt water energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

