
Wetenschap
Waterstofbinding:moleculen identificeren die deze interactie niet vormen
Waterstofbinding begrijpen
Waterstofbinding is een speciaal type dipool-dipoolinteractie die optreedt wanneer:
1. Waterstof (H) is direct gebonden aan een zeer elektronegatief atoom (zoals zuurstof (O), stikstof (N) of fluor (F)).
2. Het waterstofatoom wordt aangetrokken door een eenzaam elektronenpaar op een ander zeer elektronegatief atoom in een nabijgelegen molecuul.
Voorbeelden:
* Water (H₂O): De H-atomen zijn gebonden aan O, en de O heeft alleenstaande paren, dus water vormt sterke waterstofbruggen.
* Ammoniak (NH₃): De H-atomen zijn gebonden aan N en de N heeft een eenzaam paar, waardoor waterstofbinding mogelijk is.
* Methanol (CH₃OH): Het H-atoom dat aan de O is gehecht, kan waterstofbruggen vormen.
Het molecuul dat geen waterstofbinding vertoont
Het molecuul dat dat niet doet waterstofbruggen vertonen is methaan (CH₄) .
Dit is waarom:
* Geen sterk elektronegatieve atomen: Methaan heeft alleen koolstof- en waterstofatomen. Geen van deze elementen is zeer elektronegatief.
* Geen alleenstaande paren: Het koolstofatoom in methaan heeft geen enkele elektronenparen die kunnen deelnemen aan waterstofbruggen.
Laat het me weten als je meer voorbeelden wilt zien!
 Wat is de formule voor ionische verbinding gevormd tussen natrium en jodium?
Wat is de formule voor ionische verbinding gevormd tussen natrium en jodium?  Licht en nanodeeltjes tegen kanker
Licht en nanodeeltjes tegen kanker Wat is de moleculaire geometrie van stikstoftribromide?
Wat is de moleculaire geometrie van stikstoftribromide?  Welk effect heeft een solide niet -ioniserende opgeloste stof op het vriespunt van oplosmiddel?
Welk effect heeft een solide niet -ioniserende opgeloste stof op het vriespunt van oplosmiddel?  Geabsorbeerde fotonen door 2-oxocarbonzuren omzetten in zeer reactieve singlet-zuurstof
Geabsorbeerde fotonen door 2-oxocarbonzuren omzetten in zeer reactieve singlet-zuurstof
Hoofdlijnen
- Alle genen die zich op een bepaald chromosoom bevinden, omvatten A?
- Hoe worden ecosystemen en biomen verbonden?
- Wat is de definitie van voedselcyclus?
- Wat is de biologie van de organisme?
- Waarom hebben planten een gezond wortelsysteem nodig voor fotosynthese?
- Wat zijn enkele biologiegerelateerde banen?
- Nieuwe vogelsoort genoemd naar Harvard-vader van biodiversiteit
- Is een cel zonder kern genaamd prokaryotische cel?
- Hoe is het centrum van een chromosomen genoemd?
- Op hematiet gebaseerde nanodraadstructuren om de conversie van zonne-energie naar brandstof bij foto-elektrochemische watersplitsing te verbeteren

- Nieuw biokatalytisch systeem zet afvalbiomassa om in chemicaliën met toegevoegde waarde
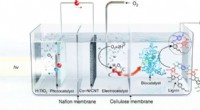
- Levenscyclusanalyse lokaliseert duurzaamheidshotspots in biochemische productie

- Met metaaloxide doordrenkte membranen kunnen een energiezuinig alternatief bieden voor chemische scheidingen

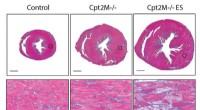
- Onderzoek toont aan dat vette brandstof nodig is om cardiale hypertrofie om te keren
 Waarom komt een lichtstraal incident op rechthoekig glazen plaat ondergedompeld in elk medium, even parallel aan zichzelf?
Waarom komt een lichtstraal incident op rechthoekig glazen plaat ondergedompeld in elk medium, even parallel aan zichzelf?  Welke weerstand tegen de beweging van een object?
Welke weerstand tegen de beweging van een object?  Hoe vertegenwoordigt u de beweging van energie via een ecosysteem?
Hoe vertegenwoordigt u de beweging van energie via een ecosysteem?  Wat gebeurt er met de kracht tussen geladen en niet -beschuldigde objecten naarmate de afstand afneemt?
Wat gebeurt er met de kracht tussen geladen en niet -beschuldigde objecten naarmate de afstand afneemt?  Is een goede aanwezigheid gelijk aan cijfers?
Is een goede aanwezigheid gelijk aan cijfers?  Halfgeleiderapparaten met een brede bandgap op basis van siliciumcarbide kunnen een revolutie teweegbrengen in de elektronica
Halfgeleiderapparaten met een brede bandgap op basis van siliciumcarbide kunnen een revolutie teweegbrengen in de elektronica Welke elementen gevonden in de vrije elementaire staat?
Welke elementen gevonden in de vrije elementaire staat?  Waarom lijken jonge planten en dieren op hun ouders?
Waarom lijken jonge planten en dieren op hun ouders?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

