
Wetenschap
Berekening van de pH van een natriumcyanide (NaCN) oplossing:een stapsgewijze handleiding
De chemie begrijpen
* NaCN is het zout van een zwak zuur (HCN) en een sterke base (NaOH). Dit betekent dat de oplossing basisch zal zijn.
* Het CN⁻-ion hydrolyseert in water, reageren met water om hydroxide-ionen (OH⁻) te produceren en de oplossing basisch te maken.
De stappen
1. Schrijf de hydrolysereactie op:
CN⁻(aq) + H₂O(l) ⇌ HCN(aq) + OH⁻(aq)
2. Een ICE-tabel instellen (Initial, Change, Equilibrium):
| | CN⁻ | HCN | OH⁻ |
|------------|-----------|----------|-----------|
| Initiële | 0,028 M | 0 | 0 |
| Wijzig | -x | +x | +x |
| Evenwicht | 0,028x | x | x |
3. Schrijf de Kb-expressie:
Kb =([HCN][OH⁻]) / [CN⁻]
4. Bereken Kb:
Kw =Ka * Kb
Kb =Kw / Ka =(1,0 x 10⁻¹⁴) / (4,9 x 10⁻¹⁰) =2,04 x 10⁻⁵
5. Vervang de evenwichtsconcentraties in de Kb-uitdrukking:
2,04 x 10⁻⁵ =(x * x) / (0,028 - x)
6. Aangezien Kb klein is, kunnen we aannemen dat x verwaarloosbaar is vergeleken met 0,028:
2,04 x 10⁻⁵ ≈ (x²) / 0,028
7. Los x op (wat [OH⁻] vertegenwoordigt):
x² ≈ 2,04 x 10⁻⁵ * 0,028
x ≈ √(2,04 x 10⁻⁵ * 0,028)
x ≈ 7,54 x 10⁻⁴ M
8. Bereken pOH:
pOH =-log[OH⁻] =-log(7,54 x 10⁻⁴) ≈ 3,12
9. Bereken de pH:
pH + pOH =14
pH =14 - pOH ≈ 14 - 3,12 ≈ 10,88
Daarom is de pH van een 0,028 M NaCN-oplossing ongeveer 10,88.
 Nieuw type triterpenen ontdekt
Nieuw type triterpenen ontdekt Wanneer moleculen van een gebied van hoge concentratie naar laag gaan, met de?
Wanneer moleculen van een gebied van hoge concentratie naar laag gaan, met de?  Geef de formule van ionen aanwezig in natriumfosfaat?
Geef de formule van ionen aanwezig in natriumfosfaat?  Supramoleculaire lijm met bruikbaar temperatuurbereik van 400 graden Celsius
Supramoleculaire lijm met bruikbaar temperatuurbereik van 400 graden Celsius Chemici ontwikkelen een eenvoudige, gebruiksvriendelijke methode om verontreinigende stoffen in water af te breken
Chemici ontwikkelen een eenvoudige, gebruiksvriendelijke methode om verontreinigende stoffen in water af te breken
 Waarom bestaan er cruciale culturele verschillen tussen landen?
Waarom bestaan er cruciale culturele verschillen tussen landen?  Naarmate onze planeet groener wordt, planten vertragen de opwarming van de aarde
Naarmate onze planeet groener wordt, planten vertragen de opwarming van de aarde Luierwissel:Nederlanders veranderen luiers in meubels
Luierwissel:Nederlanders veranderen luiers in meubels Betrouwbaar tropisch weerpatroon om te veranderen in een opwarmend klimaat
Betrouwbaar tropisch weerpatroon om te veranderen in een opwarmend klimaat Hoe hebben de pioniers natuurlijke hulpbronnen gebruikt om aan hun behoeften te voldoen?
Hoe hebben de pioniers natuurlijke hulpbronnen gebruikt om aan hun behoeften te voldoen?
Hoofdlijnen
- Wat zijn de 6 soort gegevens die worden gebruikt om een organisme te classificeren?
- Welke vorm is tijdens interfase het DNA?
- Noem elk ander type maagklier en de producten die ze produceren?
- Waar zijn DNA -cellen van gemaakt?
- Wetenschappers ontdekken hoe planten grote wortelziekten bestrijden
- Welke twee moleculen gebruiken planten om glucose te maken?
- Brengt glucose een cel binnen of verlaat hij een cel?
- Hoeveel chromosomen heeft een spinwortelplant?
- Welke organel dient als het controlecentrum voor celmetabolisme en reproductie?
- Onderzoekers leggen in realtime rondzwervende moleculaire fragmenten vast

- Brandstof en chemicaliën uit plantaardig afval

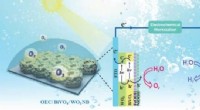
- Verbetering van de prestaties voor efficiënte foto-elektrochemische watersplitsing
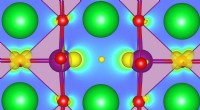
- Onderzoekers verbeteren de beschrijving van defecte oxiden met de eerste principes-berekening
- Wetenschappers onthullen dynamische zilverkristallisatie door in-situ SEM

 Wat is een fanisfeer?
Wat is een fanisfeer?  Wat absorbeert negatieve energie?
Wat absorbeert negatieve energie?  Bepalen lichtgolffrequenties welke kleur je ziet?
Bepalen lichtgolffrequenties welke kleur je ziet?  Punten op een bol of hoeken in de cirkel worden gemeten eenheden genoemd?
Punten op een bol of hoeken in de cirkel worden gemeten eenheden genoemd?  Handdesinfecterend middel is geweldig in het bewaren van insecten-DNA
Handdesinfecterend middel is geweldig in het bewaren van insecten-DNA  Krachtige voorspelling:een betere manier vinden om de orkaansterkte te voorspellen
Krachtige voorspelling:een betere manier vinden om de orkaansterkte te voorspellen As van vulkanen uit het dinosaurustijdperk verbonden met schalieolie, gas-
As van vulkanen uit het dinosaurustijdperk verbonden met schalieolie, gas- Hoe wordt de massa van een lichaam beïnvloed tijdens het opladen?
Hoe wordt de massa van een lichaam beïnvloed tijdens het opladen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

