
Wetenschap
Geleidbaarheid van zilvernitraat:de eigenschappen ervan begrijpen
Dit is waarom:
* Ionische verbinding: Zilvernitraat is een ionische verbinding, wat betekent dat het is gemaakt van positief geladen zilverionen (Ag+) en negatief geladen nitraationen (NO3-).
* Solid State: In vaste toestand worden de ionen stevig vastgehouden in een kristalroosterstructuur. De ionen kunnen niet vrij bewegen, dus er is geen ladingsstroom en dus geen geleidbaarheid.
Zilvernitraat wordt echter een sterke geleider als het in water wordt opgelost:
* Dissociatie: Wanneer opgelost in water, breken de ionische bindingen in zilvernitraat en kunnen de ionen vrij bewegen. Dit proces wordt dissociatie genoemd.
* Elektrolyt: De oplossing bevat nu een hoge concentratie mobiele ionen, waardoor het een sterke elektrolyt is. Dit betekent dat het elektriciteit zeer goed kan geleiden.
Samengevat:
* Vast zilvernitraat: Geen dirigent
* Waterige zilvernitraatoplossing: Een sterke dirigent
 Wat het kwikbesluit van de EPA betekent voor de volksgezondheid
Wat het kwikbesluit van de EPA betekent voor de volksgezondheid  De hittegolven van tegenwoordig voelen veel heter aan dan de hitte-index aangeeft
De hittegolven van tegenwoordig voelen veel heter aan dan de hitte-index aangeeft Waren allemaal in grote problemen:klimaatpanel ziet een moeilijke toekomst
Waren allemaal in grote problemen:klimaatpanel ziet een moeilijke toekomst Minimale bodemverontreiniging
Minimale bodemverontreiniging Cultureel verzet:is LGBTQ-vooruitgang een aanval op het christendom?
Cultureel verzet:is LGBTQ-vooruitgang een aanval op het christendom?
Hoofdlijnen
- Hoe weten cellen wanneer ze de celcyclus moeten doorlopen? Nieuwe studie vindt verband tussen verdeeldheid en groeisnelheid
- Een vlieg heeft twee allelen voor de kleur van zijn ogen. Het groene allel is recessief en wordt vertegenwoordigd door blauw dominant, p. Als er 28 organismen zijn, welke p?
- Wat is de term voor elk organisme dat zijn energie kan verkrijgen door ander organisme te eten?
- Master Microbiologie snel:bewezen studietechnieken voor succes
- Hoe verbeteren verbeteringen in microscooptechnologieën uw begrip van de celtheorie?
- Welke factoren beïnvloeden biomen?
- Hebben reptielen en vogels vergelijkbare levenscycli?
- Hoe heet een plantentak?
- Wat is de rol van wetenschap in de samenleving?
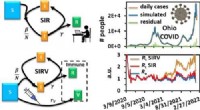
- Chemielabstudenten voorspellen verspreiding van COVID-19 met kinetische modellen
- Koolstof-12:de dominante isotoop van koolstof

- Een chemisch maatpak voor alzheimermedicijnen
- Ontdekking opent nieuwe wegen voor het ontwerpen van medicijnen om resistente malaria te bestrijden

- Video:Waarom kan ik thuis geen sterke drank distilleren?

 302 Vs. 304 roestvrij staal
302 Vs. 304 roestvrij staal  Welk deel van de lagen wordt enorme platen gesloten die op mantel drijven?
Welk deel van de lagen wordt enorme platen gesloten die op mantel drijven?  Wat is energie als hulpbron?
Wat is energie als hulpbron?  Welke twee krachten beïnvloeden de versnelling?
Welke twee krachten beïnvloeden de versnelling?  Wanneer ontdekte Eric de Red Groenland?
Wanneer ontdekte Eric de Red Groenland?  Is er een IB Physics SL -test?
Is er een IB Physics SL -test?  Welke illustreert het beste de manier waarop straling thermische energie overbrengt?
Welke illustreert het beste de manier waarop straling thermische energie overbrengt?  Test voor Benzeen
Test voor Benzeen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

