
Wetenschap
Koolstof-12:de dominante isotoop van koolstof
Door Basil Phillips – Bijgewerkt op 24 maart 2022
De kern van elk atoom bevat protonen, neutronen en elektronen. Hoewel het aantal protonen en elektronen voor een bepaald element constant is, kan het aantal neutronen variëren, waardoor verschillende isotopen ontstaan. Koolstof heeft, net als veel andere elementen, één isotoop die overweldigend vaker voorkomt dan de andere.
Koolstof‑12
Koolstof-12 is de meest voorkomende koolstofisotoop en is verantwoordelijk voor bijna 99% van de natuurlijk voorkomende koolstof op aarde. De kern bestaat uit zes protonen en zes neutronen, wat een totale massa oplevert van precies 12.000 atomaire massa-eenheden (amu). Vanwege deze exacte massa dient koolstof-12 als de internationale referentiestandaard voor alle andere atoommassa's.
Andere natuurlijk voorkomende isotopen
Naast koolstof-12 komen er in de natuur nog twee andere stabiele isotopen voor. Koolstof-13, dat zeven neutronen bevat, vertegenwoordigt ongeveer 1% van de terrestrische koolstof. Koolstof-14, met acht neutronen, is radioactief en aanwezig op een niveau van grofweg twee biljoenste van de natuurlijke koolstof. Wetenschappers hebben ook kortlevende isotopen gesynthetiseerd, variërend van koolstof-8 tot koolstof-22, maar deze onstabiele vormen hebben beperkte praktische toepassingen.
Koolstof‑13
Omdat levende organismen bij voorkeur koolstof-12 opnemen, is de verhouding koolstof-13 tot koolstof-12 in biologische materialen iets lager dan de verhouding in het milieu. Door deze verhouding in ijskernen, boomringen en mariene sedimenten te meten, kunnen wetenschappers de atmosferische kooldioxideconcentraties en de opnamesnelheden in de oceanen afleiden, wat kritische inzichten oplevert in de historische klimaatverandering.
Koolstof‑14
Koolstof-14 is uniek onder de koolstofisotopen omdat het radioactief is. Het vervalt met een halfwaardetijd van 5730 jaar, waarbij bètastraling vrijkomt. Alle levende organismen absorberen koolstof-14 via fotosynthese en ademhaling; wanneer een organisme sterft, vervalt de resterende koolstof-14 in een voorspelbaar tempo. Door de resterende koolstof-14 in oude monsters te meten, kunnen onderzoekers met opmerkelijke precisie de ouderdom van archeologische en geologische materialen bepalen – een methode die bekend staat als radiokoolstofdatering.
 Wat is het totale aantal elektronen in 2P Subblevel A chloor Atom Ground State?
Wat is het totale aantal elektronen in 2P Subblevel A chloor Atom Ground State?  Niet zo snel:sommige batterijen kunnen te ver worden geduwd
Niet zo snel:sommige batterijen kunnen te ver worden geduwd Elektronendeling in methaan- (CH₄) en water- (H₂O) moleculen
Elektronendeling in methaan- (CH₄) en water- (H₂O) moleculen  Wat is 83 gram natriumhydroxide in moedervlekken?
Wat is 83 gram natriumhydroxide in moedervlekken?  Onderzoekers verbinden eerst siliciumatomen op oppervlakken
Onderzoekers verbinden eerst siliciumatomen op oppervlakken
Hoofdlijnen
- Hoe heet een paar overeenkomstige chromosomen?
- Hoe bedreigde zoetwaterparelmossel redden?
- Waarom kan een disfunctioneel gen één type cel in het lichaam beïnvloeden, maar niet op andere typen?
- Wetenschappers ontdekken dat hogere CO₂-niveaus de overleving van virussen in de lucht vergroten en het overdrachtsrisico vergroten
- Een biosyntheseroute kan worden gekarakteriseerd als?
- Stille code van nucleotiden, geen aminozuren, bepaalt functies van vitale eiwitten
- Wat is een Syonyum?
- Wat voor soort venatie heeft de Petunia -fabriek?
- Wat gebeurt er als organismen organische verbindingen bouwen?
- Feedback van duizenden ontwerpen kan eiwittechnologie transformeren
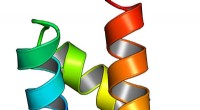
- Poreuze kristallen gebruiken om licht te oogsten
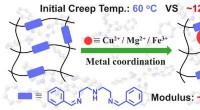
- Metaalcoördinatie maakt hoge temperatuur, kruipvast polyimine vitrimeer preparaat
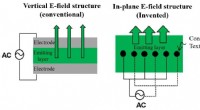
- In textielvezels ingebed multiluminescent apparaat voor toekomstige draagbare apparaten
- Belastingregel voor industrie beloont afvang van koolstof

 Wat is een soort eiwit dat chemische reacties in levende wezens versnelt?
Wat is een soort eiwit dat chemische reacties in levende wezens versnelt?  Waarom vallen bomen naar de weg?
Waarom vallen bomen naar de weg?  Wat is de uitgebalanceerde chemische vergelijking voor de ontleding van kalksteen tot calciumoxide en kooldioxide?
Wat is de uitgebalanceerde chemische vergelijking voor de ontleding van kalksteen tot calciumoxide en kooldioxide?  Wat labels op textiel ons kunnen vertellen over de samenleving
Wat labels op textiel ons kunnen vertellen over de samenleving  De kustwateren van Australië zijn rijk aan inheems cultureel erfgoed, maar het is verborgen en wordt bedreigd
De kustwateren van Australië zijn rijk aan inheems cultureel erfgoed, maar het is verborgen en wordt bedreigd Kan een slecht element in boiler absurd hoge elektrische rekeningen veroorzaken?
Kan een slecht element in boiler absurd hoge elektrische rekeningen veroorzaken?  Veeg houtas van open haard naar tuin
Veeg houtas van open haard naar tuin Waarom zijn er vulkanen op het Hawaiiaanse eiland?
Waarom zijn er vulkanen op het Hawaiiaanse eiland?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

