
Wetenschap
Zuurstofatomen in zwavelzuur:een stapsgewijze berekening
1. Bepaal de molecuulformule en molaire massa van zwavelzuur
*Zwavelzuur heeft de formule H₂SO₄.
* De molaire massa is:
* (2 x 1,008 g/mol H) + (32,066 g/mol S) + (4 x 15,999 g/mol O) =98,079 g/mol
2. Bereken het aantal mol zwavelzuur
* Deel de gegeven massa door de molaire massa:
* 17,9325 g / 98,079 g/mol =0,183 mol H₂SO₄
3. Bereken het aantal mol zuurstofatomen
* Er zijn 4 zuurstofatomen per molecuul H₂SO₄:
* 0,183 mol H₂SO₄ x (4 mol O / 1 mol H₂SO₄) =0,732 mol O
4. Bereken het aantal zuurstofatomen
* Gebruik het getal van Avogadro (6,022 x 10²³ atomen/mol) om mollen om te zetten in atomen:
* 0,732 mol O x (6,022 x 10²³ atomen/mol) =4,41 x 10²³ zuurstofatomen
Daarom zijn er ongeveer 4,41 x 10²³ zuurstofatomen in 17,9325 g zwavelzuur.
Hoofdlijnen
- Onderzoekers bouwen een biomimetisch 'zacht kanon' om te begrijpen hoe schimmelsporen worden verspreid
- Onderzoek toont aan dat regenererende wormen genetische controle hebben over hun algenpartners
- Bio-invaders:bedreigingen voor ecosystemen begrijpen - definitie en impact
- Welke vaardigheden krijg je van de wetenschap?
- Kan het vage viraal gaan voor generatie Y?
- Elke cel in elk levend ding komt van een ander dat wat doet?
- Studie laat zien hoe vissen in de schemerzone evolueerden
- Welke vragen verzetten zich tegen evolutie?
- Een doorbraak op het gebied van cellulaire engineering:high-yield CRISPR zonder virale vectoren
- Miniatuurdruppels kunnen een raadsel over de oorsprong van het leven oplossen

- Onderzoek naar betere biotransformaties

- AI-software helpt bij het ontwerpen van nieuw materiaal voor zonnecellen
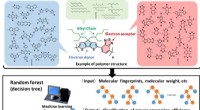
- Onderzoekers ontdekken dat ruimte tussen polymeerketens de energieconversie beïnvloedt

- Eerder onbekende kristallijne fase van halfwaterig calciumcarbonaat ontdekt

 Gebrek aan steun verlengt werkloosheid
Gebrek aan steun verlengt werkloosheid De hoeveelheid energie die een geluidsgolf vervolgt door eenheidsgebied?
De hoeveelheid energie die een geluidsgolf vervolgt door eenheidsgebied?  Wat is de beweging van een object dat wordt gezegd als zijn snelheid constant is?
Wat is de beweging van een object dat wordt gezegd als zijn snelheid constant is?  Wat zijn enkele grote landvormen?
Wat zijn enkele grote landvormen?  Zijn schimmelcellen eukaryotisch of prokaryotisch en waarom?
Zijn schimmelcellen eukaryotisch of prokaryotisch en waarom?  Hoe windenerosie kan de rots beïnvloeden?
Hoe windenerosie kan de rots beïnvloeden?  Is zilveren chloride polair of ionisch niet -polair?
Is zilveren chloride polair of ionisch niet -polair?  Hoe kunnen bacteriën zich voortplanten door splijting?
Hoe kunnen bacteriën zich voortplanten door splijting?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


