
Wetenschap
Inzicht in de zuurgraad van droog waterstofchloride (HCl)
* HCl is een polair molecuul: Het waterstofatoom heeft een gedeeltelijke positieve lading (δ+) en het chlooratoom heeft een gedeeltelijke negatieve lading (δ-) vanwege het elektronegativiteitsverschil daartussen.
* HCl kan protonen doneren (H+): Wanneer HCl in water oplost, ioniseert het onder vorming van H+-ionen (protonen) en Cl-ionen. Dit vermogen om protonen te doneren is het bepalende kenmerk van een zuur.
* Droge HCl is niet geïoniseerd: Hoewel droge HCl nog steeds protonen kan doneren, doet het dit in veel mindere mate dan wanneer het in water is opgelost. Dit komt omdat de afwezigheid van watermoleculen het ionisatieproces verhindert.
Dus hoewel droge HCl geen sterk zure eigenschappen vertoont, is het nog steeds zuur vanwege het potentieel om protonen te doneren.
Waarom wordt het "droge" HCl genoemd?
De term "droge" HCl verwijst naar het gas in zijn zuivere vorm zonder opgelost water. Als er water aanwezig is, reageert het met HCl en vormt zoutzuur (HCl(aq)), een sterk zuur.
 Verbetering van de waarneming van eiwitbinding
Verbetering van de waarneming van eiwitbinding Wat is de evenwichtige vergelijking voor kopersulfaatoplossing en ammoniakoplossing?
Wat is de evenwichtige vergelijking voor kopersulfaatoplossing en ammoniakoplossing?  Hoe vindt u hoeveel mol in een verbinding
Hoe vindt u hoeveel mol in een verbinding  Welke 5 elementen vormen eiwitmoleculen?
Welke 5 elementen vormen eiwitmoleculen?  Waarom heeft Miller een condensor in zijn experiment opgenomen wat het vertegenwoordigen model?
Waarom heeft Miller een condensor in zijn experiment opgenomen wat het vertegenwoordigen model?
 De botten van een oude Maya-ambassadeur tonen een leven vol voorrechten en ontberingen
De botten van een oude Maya-ambassadeur tonen een leven vol voorrechten en ontberingen  De studie van materie en veranderingen die zich voordoen in de beste beschrijft de wetenschap van?
De studie van materie en veranderingen die zich voordoen in de beste beschrijft de wetenschap van?  Waarom schilderen mensen de bodem van bomen wit?
Waarom schilderen mensen de bodem van bomen wit?  Hoe een vulkaan en vlammende rode zonsondergangen een amateurwetenschapper in Hawaï ertoe brachten jetstreams te ontdekken
Hoe een vulkaan en vlammende rode zonsondergangen een amateurwetenschapper in Hawaï ertoe brachten jetstreams te ontdekken Wat is een recreatieve ervaring tussen levensvormen en ecosystemen die worden genoemd?
Wat is een recreatieve ervaring tussen levensvormen en ecosystemen die worden genoemd?
Hoofdlijnen
- Factoren die het fenotype bepalen:genetica, omgeving en meer
- Wat is hetzelfde van DNA en RNA?
- Het lysosoom:het primaire recyclingcentrum van Cell
- Wat beschrijft het beste een groot verschil tussen plantencellen en dierlijke cellen?
- Wetenschappers maken een einde aan een mysterie van 50 jaar en onthullen hoe bacteriën zich kunnen verplaatsen
- Welke interacties bestaan er tussen de drie lichaamssystemen?
- Waar krijgen planten glucose en zuurstof nodig voor ademhaling?
- Hoe is classificatie en evolutie met elkaar verbonden?
- Leg uit hoe draagvermogen het aantal organisme in een ecosysteem beïnvloedt?
- Insuline sorteren en afscheiden op vervaldatum
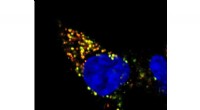
- Op maat gemaakte koolstof kan wetenschappers helpen bij het vinden van erfelijke ziekten en de juiste doses medicatie
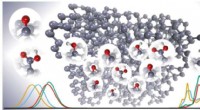
- Moleculaire machinerie die krachtige antibiotica maakt onthuld na tientallen jaren van onderzoek
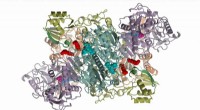
- Nieuwe katalysatoren voor betere brandstofcellen

- Tweedimensionaal MXene als nieuw elektrodemateriaal voor weergave van de volgende generatie

 Wat veroorzaakte de meest giftige algenbloei die ooit in Monterey Bay is waargenomen?
Wat veroorzaakte de meest giftige algenbloei die ooit in Monterey Bay is waargenomen? Waarom hebben planten en andere fotosynthetische organismen CO 2 uit de atmosfeer nodig?
Waarom hebben planten en andere fotosynthetische organismen CO 2 uit de atmosfeer nodig?  De percentages voor een cirkeldiagram berekenen
De percentages voor een cirkeldiagram berekenen Nieuw bewijs:de massieve ijzerrijke kern van de maan weerspiegelt die van de aarde
Nieuw bewijs:de massieve ijzerrijke kern van de maan weerspiegelt die van de aarde  Wat voor soort vragen stellen wetenschappers?
Wat voor soort vragen stellen wetenschappers?  Wat zijn de startstoffen in fotosynthese?
Wat zijn de startstoffen in fotosynthese?  Werken onze mitochondriën bij 50 graden Celsius?
Werken onze mitochondriën bij 50 graden Celsius?  Hoe kunnen de fasen van een maan op een andere planeet anders zijn?
Hoe kunnen de fasen van een maan op een andere planeet anders zijn?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

