
Wetenschap
Zuur-base-titratie:voorbeelden en toepassingen - een uitgebreide gids
Voorbeelden van zuur-base-titratie:
Zuur-base-titratie is een veelgebruikte techniek om de concentratie van een onbekende zuur- of base-oplossing te bepalen. Hier zijn enkele voorbeelden:
1. Bepalen van de concentratie van azijn:
* Onbekend: Azijn (azijnzuuroplossing)
* Bekend: Natriumhydroxideoplossing (NaOH) met bekende concentratie
* Procedure: Een bekend volume azijn wordt getitreerd met de standaard NaOH-oplossing met behulp van een pH-indicator (zoals fenolftaleïne). Het equivalentiepunt wordt bereikt wanneer de oplossing roze wordt, wat aangeeft dat al het azijnzuur heeft gereageerd met NaOH.
* Berekening: Het gebruikte volume NaOH en de concentratie ervan worden gebruikt om de concentratie azijnzuur in de azijn te berekenen.
2. Het bepalen van de sterkte van een antacidum:
* Onbekend: Antacidumtablet met een base zoals calciumcarbonaat (CaCO3)
* Bekend: Zoutzuur (HCl)-oplossing met bekende concentratie
* Procedure: Een maagzuurremmer wordt opgelost in een bekend volume HCl. De resulterende oplossing wordt vervolgens getitreerd met een standaard NaOH-oplossing. Het volume NaOH dat wordt gebruikt om de overmaat HCl te neutraliseren, geeft de hoeveelheid zuur aan die door het maagzuurremmer wordt geneutraliseerd.
* Berekening: De hoeveelheid zuur die door de antacidum wordt geneutraliseerd, wordt gebruikt om het "zuurneutraliserende vermogen" van de antacidum te bepalen.
3. Bepalen van de concentratie van een zwak zuur:
* Onbekend: Zwakke zure oplossing zoals azijnzuur (CH3COOH)
* Bekend: Sterke basische oplossing zoals natriumhydroxide (NaOH) met bekende concentratie
* Procedure: Een bekend volume van de zwakzure oplossing wordt getitreerd met de standaard NaOH-oplossing met behulp van een pH-indicator. Het equivalentiepunt wordt bereikt wanneer de oplossing roze kleurt.
* Berekening: Het gebruikte volume NaOH en de concentratie ervan worden gebruikt om de concentratie van het zwakke zuur te berekenen.
4. De concentratie van een sterke basis bepalen:
* Onbekend: Sterke basische oplossing zoals kaliumhydroxide (KOH)
* Bekend: Sterke zuuroplossing zoals zoutzuur (HCl) met bekende concentratie
* Procedure: Een bekend volume van de sterke basische oplossing wordt getitreerd met de standaard HCl-oplossing met behulp van een pH-indicator. Het equivalentiepunt wordt bereikt wanneer de oplossing geel wordt.
* Berekening: Het gebruikte volume HCl en de concentratie ervan worden gebruikt om de concentratie van de sterke base te berekenen.
5. Het meten van de hoeveelheid zuur in wijn:
* Onbekend: Wijn (bevat wijnsteenzuur)
* Bekend: Natriumhydroxideoplossing (NaOH) met bekende concentratie
* Procedure: Een bekend volume wijn wordt getitreerd met de standaard NaOH-oplossing met behulp van een pH-indicator. Het equivalentiepunt wordt bereikt wanneer de oplossing roze kleurt.
* Berekening: Het gebruikte volume NaOH en de concentratie ervan worden gebruikt om de hoeveelheid wijnsteenzuur in de wijn te berekenen.
Dit zijn slechts enkele voorbeelden, maar zuur-base-titratie heeft vele toepassingen op verschillende gebieden, zoals:
* Chemie: het bepalen van de concentratie van zuren en basen, het verifiëren van chemische reacties en het analyseren van onbekende stoffen.
* Voedingswetenschap: het analyseren van de zuurgraad van voedingsmiddelen zoals azijn, wijn en sap.
* Milieuwetenschappen: het analyseren van de zuurgraad van watermonsters.
* Geneeskunde: het meten van de zuurgraad van lichaamsvloeistoffen zoals bloed en urine.
Het begrijpen van de principes van zuur-base-titratie en de toepassingen ervan is cruciaal voor een breed scala aan wetenschappelijke en industriële processen.
 Supergeleiding:waarom moet het zo koud zijn?
Supergeleiding:waarom moet het zo koud zijn?  Waarom krijgen de atomen een grotere doorsnede als je naar groep 1 gaat?
Waarom krijgen de atomen een grotere doorsnede als je naar groep 1 gaat?  Stapsgewijze handleiding voor het bereiden van een steriele natriumchlorideoplossing
Stapsgewijze handleiding voor het bereiden van een steriele natriumchlorideoplossing  Als het mengsel van elektrisch neutraal hoeveel meer bèta -deeltjes dan alfa in ballon zijn?
Als het mengsel van elektrisch neutraal hoeveel meer bèta -deeltjes dan alfa in ballon zijn?  Wat is het totale aantal valentie -elektronen in een fluoratoom die u n grondtoestand?
Wat is het totale aantal valentie -elektronen in een fluoratoom die u n grondtoestand?
 Amerikaanse mijnbouwlocaties dumpen dagelijks 50 miljoen gallons vervuild afvalwater
Amerikaanse mijnbouwlocaties dumpen dagelijks 50 miljoen gallons vervuild afvalwater Onderzoek onthult dat veel staatsparken in de Grote Meren getroffen zijn door recordhoge waterstanden
Onderzoek onthult dat veel staatsparken in de Grote Meren getroffen zijn door recordhoge waterstanden Hoe zijn de 6 stappen van wetenschappelijk onderzoek gerelateerd?
Hoe zijn de 6 stappen van wetenschappelijk onderzoek gerelateerd?  Wat betekent klimatologische stress?
Wat betekent klimatologische stress?  As You Go Dieper in the Earth Wat gebeurt er met de dichtheid van de lagen?
As You Go Dieper in the Earth Wat gebeurt er met de dichtheid van de lagen?
Hoofdlijnen
- Welk proces met welke niet -gerelateerde organismen komen op elkaar komen opgeroepen?
- Welke tak is herpetoloog in het leven op aarde of fysieke wetenschap?
- Hoe consumeert een cel voedseldeeltje dat het te groot is om het eiwitkanaal te passeren?
- Wat zijn de twee brede categorieën cellen?
- Panspermia:zorgden buitenaardse zaden ervoor dat het leven op aarde explodeerde?
- Ziekteverwekkers identificeren die sojastamkanker veroorzaken
- Hebben rivieren de evolutie van Sumatraanse cascadekikkers beïnvloed?
- Komt cellulaire ademhaling op in plantencellen?
- Cellen die geen kern hebben?
- Een lasergestuurde programmeerbare contactloze transferdruktechniek

- Goedkoop, efficiënte en stabiele foto-elektrode kan de watersplitsing met zonne-energie verbeteren

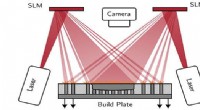
- Holografische bundelvorming om metallic 3D-printen een boost te geven
- Massaspectrometriebeeldvorming maakt ingrediënten, additieven en contaminanten van voedsel zichtbaar

- Nieuw onderzoeksgebied:Hoe eiwitstructuren veranderen door normaalkrachten
 Hoe werkt het leven en niet-levende dingen van een ecosysteem samen?
Hoe werkt het leven en niet-levende dingen van een ecosysteem samen?  Waarom zijn zonnevlekken een bron van radio-emissies? Onderzoeker legt meer uit
Waarom zijn zonnevlekken een bron van radio-emissies? Onderzoeker legt meer uit  Hoe beschadigen of vernietigen erosie, uitputting van voedingsstoffen en woestijnvorming de bodem?
Hoe beschadigen of vernietigen erosie, uitputting van voedingsstoffen en woestijnvorming de bodem?  Welke bewegingswet legt uit hoe raketten in de ruimte worden gelanceerd?
Welke bewegingswet legt uit hoe raketten in de ruimte worden gelanceerd?  Wetenschappers fotograferen zelfassemblage van nanodeeltjes
Wetenschappers fotograferen zelfassemblage van nanodeeltjes Wat is koolstofdioxide geproduceerd door beide processen?
Wat is koolstofdioxide geproduceerd door beide processen?  Kennis opdoen door vereenvoudiging
Kennis opdoen door vereenvoudiging Wat is iriserend.?
Wat is iriserend.?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

