
Wetenschap
Het schatten van de energie om bindingen in 2-buteen te verbreken:een stapsgewijze handleiding
1. Identificeer de obligaties:
* 2-buteen heeft één dubbele koolstof-koolstofbinding (C=C) en vijf enkele koolstof-waterstofbindingen (C-H).
2. Bereken de energie voor de dubbele binding:
* De gemiddelde bindingsenthalpie voor een C=C-binding is 614 kJ/mol.
3. Bereken de energie voor de afzonderlijke obligaties:
* De gemiddelde bindingsenthalpie voor een C-H-binding is 348 kJ/mol.
* Omdat er 5 C-H-bindingen zijn, is de totale energie die nodig is om ze te verbreken 5 * 348 kJ/mol =1740 kJ/mol.
4. Totale energie:
* Om alle bindingen in 2-buteen te verbreken, moet je de energie voor de dubbele binding en de enkele bindingen bij elkaar optellen:614 kJ/mol + 1740 kJ/mol =2354 kJ/mol.
Daarom is de geschatte energie die nodig is om alle bindingen in 2-buteen te verbreken 2354 kJ/mol.
Belangrijke opmerking: Dit is een geschatte waarde. De daadwerkelijk benodigde energie kan enigszins variëren, afhankelijk van het specifieke molecuul en zijn omgeving.
 Hoe Polycomb repressieve deubiquitinase specifiek de ubiquitinatie van H2AK119 op het nucleosoom verwijdert
Hoe Polycomb repressieve deubiquitinase specifiek de ubiquitinatie van H2AK119 op het nucleosoom verwijdert  Natriumion (Na⁺):Ionvorming begrijpen
Natriumion (Na⁺):Ionvorming begrijpen  Wat zijn de hoeveelheden rode en blauwe lakmus als een oplossing neutraal?
Wat zijn de hoeveelheden rode en blauwe lakmus als een oplossing neutraal?  Lab ontwikkelt grafeenelektrode met twee oppervlakken om water te splitsen in waterstof en zuurstof
Lab ontwikkelt grafeenelektrode met twee oppervlakken om water te splitsen in waterstof en zuurstof Is crushed ijs een zuivere stof of mengsel en homogeen heterogeen?
Is crushed ijs een zuivere stof of mengsel en homogeen heterogeen?
 Zou een diep-aardse watercyclus ons begrip van planetaire evolutie veranderen?
Zou een diep-aardse watercyclus ons begrip van planetaire evolutie veranderen? Wat zijn de oorzaken van overmatig vissen?
Wat zijn de oorzaken van overmatig vissen?  Wat is principe?
Wat is principe?  Het Amerikaanse grondwater wordt zouter – wat dat betekent voor de infrastructuur, ecosystemen en de menselijke gezondheid
Het Amerikaanse grondwater wordt zouter – wat dat betekent voor de infrastructuur, ecosystemen en de menselijke gezondheid  Beschrijf welke zoogdieren in de quaternaire periode geconfronteerd werden?
Beschrijf welke zoogdieren in de quaternaire periode geconfronteerd werden?
Hoofdlijnen
- Hoe reageert het organisme op veranderingen op korte termijn in de omgeving?
- Wat zijn witte bloedcellen die pathogenen kunnen overspoelen?
- Uit onderzoek blijkt hoe lysozymeiwit in tranen gevaarlijke bacteriën vernietigt
- Waarom geeft chloroplast plantencellen het voordeel ten opzichte van dierencel?
- Waarom astronauten in de ruimte niet kunnen boeren (en hoe ze daarmee omgaan)
- Wat is de functie van lymfeklieren?
- Waarom banken hun buitenlandse activa niet voldoende diversifiëren
- Wat is het belang van cross-over in procesevolutie?
- Maakt Koud U Slaperig?
- Goedkope waterbehandeling

- Efficiënte en duurzame materialen voor perovskiet-zonnecellen

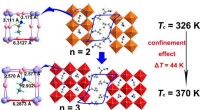
- Onderzoekers verwerven gelaagde metaalhalogenide-ferro-elektriciteit met hoge Curie-temperatuur via kooi-begrensde ethylaminerotators
- Heeft komeetinslagen het leven op aarde een boost gegeven?

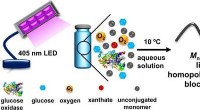
- Ultrazware precisiepolymeren
 Wat zou er gebeuren als er geen wrijving was tussen een rollende bal en de grond?
Wat zou er gebeuren als er geen wrijving was tussen een rollende bal en de grond?  Vindt er een chemische verandering plaats wanneer een stof van fase verandert?
Vindt er een chemische verandering plaats wanneer een stof van fase verandert?  Wat zijn 3 door de mens gemaakte functies die een topografische kaart hebben getoond?
Wat zijn 3 door de mens gemaakte functies die een topografische kaart hebben getoond?  Welke is kleinere zetmeelkorrel of tracheale cel?
Welke is kleinere zetmeelkorrel of tracheale cel?  Wat is de alfa-vervalvergelijking voor polonium-218?
Wat is de alfa-vervalvergelijking voor polonium-218?  Wanneer gesmolten rots koelt of hard wordt in het aardoppervlak, vormt het dan?
Wanneer gesmolten rots koelt of hard wordt in het aardoppervlak, vormt het dan?  Hoe ver van de aarde is de ster Wezn?
Hoe ver van de aarde is de ster Wezn?  Wat voorkomt ons dat we in de lucht drijven en planeten in een baan rond de zon?
Wat voorkomt ons dat we in de lucht drijven en planeten in een baan rond de zon?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

