
Wetenschap
Metaalgeleiding begrijpen:waarom metalen uitblinken in het geleiden van elektriciteit en warmte
1. De "Zee van Elektronen":
* Metaalbinding: Bij metalen zijn de buitenste elektronen van de atomen losjes gebonden en kunnen ze gemakkelijk loskomen van de atomen. Deze losgemaakte elektronen vormen een "zee" van gedelokaliseerde elektronen die vrij door de structuur van het metaal kunnen bewegen.
* Vrije elektronen: In tegenstelling tot andere materialen waar elektronen stevig gebonden zijn aan individuele atomen, zijn deze vrije elektronen niet geassocieerd met een specifiek atoom. Ze fungeren als ladingdragers.
2. Geleiding uitgelegd:
* Elektrische geleiding: Wanneer er een spanning over een metaal wordt aangelegd, worden de vrije elektronen aangetrokken door de positieve pool en afgestoten door de negatieve pool. Dit veroorzaakt een stroom van elektronen, waardoor een elektrische stroom ontstaat. Het gemak waarmee deze elektronen bewegen, bepaalt de geleidbaarheid van het metaal.
* Thermische geleiding: Wanneer warmte wordt toegepast op een metaal, absorberen de vrije elektronen energie en bewegen ze sneller, waarbij ze in botsing komen met andere elektronen en atomen. Deze energieoverdracht door botsingen verspreidt de warmte door het metaal.
Factoren die de geleidbaarheid beïnvloeden:
* Type metaal: Verschillende metalen hebben verschillende aantallen vrije elektronen en verschillende niveaus van weerstand tegen elektronenbeweging. Zilver is bijvoorbeeld de beste geleider, gevolgd door koper, goud en aluminium.
* Temperatuur: Hogere temperaturen verhogen de trilling van atomen, waardoor het moeilijker wordt voor elektronen om vrij te stromen. Dit leidt tot een hogere weerstand en een lagere geleidbaarheid.
* Onzuiverheden: Onzuiverheden in het metaal kunnen de stroom vrije elektronen verstoren, waardoor de weerstand toeneemt en de geleidbaarheid afneemt.
Samengevat: De aanwezigheid van een ‘zee’ van gedelokaliseerde elektronen in metalen zorgt voor een gemakkelijke stroom van zowel elektriciteit als warmte, waardoor ze uitstekende geleiders zijn. Dit is een fundamentele eigenschap die metalen essentieel maakt in veel toepassingen, van elektrische bedrading tot kookgerei.
Hoofdlijnen
- Wat is bevestigd aan membraansystemen en verspreid in het cytoplasma synthetiseren eiwitten?
- Hoe helpt Mimicry de kans op het overleven van een organismen te vergroten?
- Wat vereist een gastheercel om zich te voortplanten?
- Waarom is geen cellulaire energie vereist om het passagiersmolecuul door dragermolecuul over celmembraan te dragen?
- Wat is een organisme dat langzaam groeit in de kou, maar een optimale groeitemperatuur van 32 graden Celsius heeft?
- Hoe zal klimaatverandering het geografische bereik van salamandersoorten in de VS en Canada beïnvloeden?
- Roofzuchtige bacteriën die patrijspoorten maken en fresco's schilderen in schadelijke bacteriën
- Het behoud van Jaguar hangt af van de houding van de buren
- Bacteriën en virussen infecteren onze cellen via suikers:nu willen onderzoekers weten hoe ze dat doen
- Polymeer om ammoniakvervuiling op te vangen gerealiseerd

- Nieuwe methode versnelt ontwikkeling medicatie

- Wetenschappers ontwikkelen sondes die zijn ontworpen om de fysieke krachten in levende cellen te onthullen; een wereldprimeur

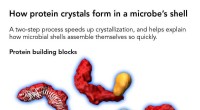
- Wetenschappers ontdekken hoe eiwitten kristallen vormen die een microbenomhulsel betegelen
- Het produceren van ammoniak via elektrochemische processen kan de uitstoot van kooldioxide verminderen

 De snelheid van een mechanische golf is afhankelijk van?
De snelheid van een mechanische golf is afhankelijk van?  Warmer, natter klimaat kan sterker betekenen, meer intense stormen
Warmer, natter klimaat kan sterker betekenen, meer intense stormen Welke stoffen worden rood lakmoespapier blauw?
Welke stoffen worden rood lakmoespapier blauw?
De eenvoudigste manier om de pH van een stof vast te stellen - om erachter te komen of het zuur of alkalisch is - is om rode en blauwe lakmoespapier te gebruiken. Rood lakmoespapier reageert op alkalis
 Welke delen van de fosforcyclus zijn geologisch?
Welke delen van de fosforcyclus zijn geologisch?  Hebben gassen een bepaalde vorm en volume? Waar of niet waar?
Hebben gassen een bepaalde vorm en volume? Waar of niet waar?  In een geïsoleerd systeem - elk fiets 1 en 2 met de massa van 30 kg botsingsfiets bewoog naar rechts bij MS terwijl links 4 Wat is de magnitude hun momentum?
In een geïsoleerd systeem - elk fiets 1 en 2 met de massa van 30 kg botsingsfiets bewoog naar rechts bij MS terwijl links 4 Wat is de magnitude hun momentum?  Waarom consumenten slechte financiële beslissingen nemen en hoe ze kunnen helpen
Waarom consumenten slechte financiële beslissingen nemen en hoe ze kunnen helpen  Welke eigenschap van water laat planten uit de grond halen door hun wortels en stengel?
Welke eigenschap van water laat planten uit de grond halen door hun wortels en stengel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


