
Wetenschap
Chloorreacties:kleurveranderingen observeren met bromide- en jodide-ionen
De reactie van chloor met bromide-ionen
* Reactie: Chloor (Cl₂) is een sterker oxidatiemiddel dan broom (Br₂). Wanneer chloor reageert met bromide-ionen (Br⁻), oxideert het de bromide-ionen tot broom.
* Kleurverandering: De oplossing verandert van kleurloos (bromide-ionen) naar oranjebruin (broom).
* Vergelijking: Cl₂(aq) + 2Br⁻(aq) → 2Cl⁻(aq) + Br₂(aq)
De reactie van chloor met jodide-ionen
* Reactie: Chloor (Cl₂) is een sterker oxidatiemiddel dan jodium (I₂). Wanneer chloor reageert met jodide-ionen (I⁻), oxideert het de jodide-ionen tot jodium.
* Kleurverandering: De oplossing verandert van kleurloos (jodide-ionen) naar bruinrood (jodium).
* Vergelijking: Cl₂(aq) + 2I⁻(aq) → 2Cl⁻(aq) + I₂(aq)
Belangrijkste punt: Deze reacties tonen de relatieve sterkte van de halogenen als oxidatiemiddelen aan. Chloor is het sterkst, gevolgd door broom en vervolgens jodium.
 Wat is de chemische formule voor zilvernatriumsulfide?
Wat is de chemische formule voor zilvernatriumsulfide?  SO2 Moleculaire geometrie:de gebogen vorm begrijpen
SO2 Moleculaire geometrie:de gebogen vorm begrijpen  Als een verbinding bestaat uit twee vloeibare elementen, is het dan zeker dat deze vloeibaar zal zijn?
Als een verbinding bestaat uit twee vloeibare elementen, is het dan zeker dat deze vloeibaar zal zijn?  Wat zijn de belangrijkste oorzaken van erosie en depositie door verwering?
Wat zijn de belangrijkste oorzaken van erosie en depositie door verwering?  Waarom zijn citroenen zuur?
Waarom zijn citroenen zuur?
 Feiten over de Great Plains
Feiten over de Great Plains Wat is een organisch materiaal zoals bladeren en twijgen die kunnen worden veranderd in humus door het ontbinden van organismen die worden genoemd?
Wat is een organisch materiaal zoals bladeren en twijgen die kunnen worden veranderd in humus door het ontbinden van organismen die worden genoemd?  Onderzoekers onthullen dat Amerikaanse maïsgewassen gevoeliger worden voor droogte
Onderzoekers onthullen dat Amerikaanse maïsgewassen gevoeliger worden voor droogte Een steen, overslaan en een sprong weg van het redden van een baai
Een steen, overslaan en een sprong weg van het redden van een baai Wat betekent ‘androgynie’ vandaag de dag?
Wat betekent ‘androgynie’ vandaag de dag?
Hoofdlijnen
- Wat is een eetbare leliebol?
- Wat is de plantenclassificatiesleutel?
- Hoe wordt de studie van afval genoemd?
- De langste mensen ter wereld delen deze merkwaardige eigenschappen
- Orchideeënplanten voeden hun zaailingen via een gedeeld ondergronds schimmelnetwerk, zo blijkt uit onderzoek
- Waarom graangewassen beter zijn
- Welke klier scheidt somatostatine uit?
- Hoe wetenschappers doen wetenschap?
- Wat zijn de drie processen die niet kunnen worden gebruikt om een vraag te beantwoorden die wetenschappers zich zouden kunnen stellen?
- Nieuw onderzoek zet glucosetransporteiwitten om in wateroplosbare vorm
- Next-gen 3D-geprinte katalysatoren om hypersonische vlucht voort te stuwen

- Een prebiotische route naar DNA
- Nieuw glow-in-the-dark materiaal kan pad van drugs door het menselijk lichaam volgen

- Elektronische grensvlaktoestand die de waterstofopslagcapaciteit in Pd-MOF-materialen verbetert
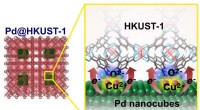
 Wat is de studie van materie en energie -interacties tussen twee door krachtenbewegingen die bekend staan als?
Wat is de studie van materie en energie -interacties tussen twee door krachtenbewegingen die bekend staan als?  Het organisme Acer Rubrum is het meest verbonden met wat?
Het organisme Acer Rubrum is het meest verbonden met wat?  Wat kan er van koolstof gemaakt worden?
Wat kan er van koolstof gemaakt worden?  Wat toont een taartvormig deel van de aarde?
Wat toont een taartvormig deel van de aarde?  Wat betekent onderhoud?
Wat betekent onderhoud?  Asteroïde scheert op 12 oktober langs de aarde:ESA (update)
Asteroïde scheert op 12 oktober langs de aarde:ESA (update) Ingenieurs zetten tienduizenden kunstmatige hersensynapsen op een enkele chip
Ingenieurs zetten tienduizenden kunstmatige hersensynapsen op een enkele chip Wat is de definitie van variabele in wetenschappelijke methode?
Wat is de definitie van variabele in wetenschappelijke methode?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

