
Wetenschap
SO2 Moleculaire geometrie:de gebogen vorm begrijpen
* Centraal Atoom: Zwavel (S) is het centrale atoom.
* Valentie-elektronen: Zwavel heeft 6 valentie-elektronen en elk zuurstofatoom heeft 6 valentie-elektronen.
* Verbinding: Zwavel vormt dubbele bindingen met elk zuurstofatoom en deelt twee elektronen met elke zuurstof.
* Eenzame paren: Zwavel heeft ook één eenzaam elektronenpaar.
* Elektronenpaarafstoting: De elektronenparen (zowel bindende als alleenstaande paren) rond het zwavelatoom stoten elkaar af. Deze afstoting leidt tot een gebogen vorm, waardoor de afstoting tussen de elektronen wordt geminimaliseerd.
Daarom heeft het SO₂-molecuul een gebogen vorm met een bindingshoek van ongeveer 119 graden.
Hoofdlijnen
- Orgelfysiologie is als grove anatomie?
- Verschillen mannelijke en vrouwelijke dinosaurussen? Een nieuwe statistische techniek helpt bij het beantwoorden van de vraag
- Kan een naaimachine DNA aan elkaar naaien?
- Wat is de betekenis van de biologie van reproductieve klonen?
- Wat is whisky-schimmel en is het gevaarlijk?
- Is een aanpassing in de biologie gemaakt door keuze of is deze geërfd?
- Wat is biologisch tijdperk?
- Hoe heet bacteriën?
- Welk deel van de cel regelt procesmitose?
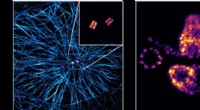
- Vooruitgang in superresolutiemicroscopie
- Een zeer gevoelig SERS-substraat voor gasdetectie

- Galvaniseren:de geboorte van een enkele kern vastgelegd in de camera

- Hoe beïnvloeden stromingskrachten van geladen oppervlakken/deeltjes en oppervlakteactieve stoffen in vloeistoffen?

- Studie initieert chemische reacties door materialen te koelen in plaats van ze te verwarmen
 Welke cellen reproduceren zich door ontluikende gist?
Welke cellen reproduceren zich door ontluikende gist?  De alkalische aardes worden geassocieerd met welke groep?
De alkalische aardes worden geassocieerd met welke groep?  Wat zijn genotype -symbolen?
Wat zijn genotype -symbolen?  Hoe is Dimorphos ontstaan?
Hoe is Dimorphos ontstaan?  Hoe het volume water in een vierkant te berekenen Tank
Hoe het volume water in een vierkant te berekenen Tank Molecuuleigenschappen veranderen door licht
Molecuuleigenschappen veranderen door licht Een samengestelde machine maken voor een 3e-graads wetenschapsproject
Een samengestelde machine maken voor een 3e-graads wetenschapsproject Jaar van extremen voor krimpende Zwitserse gletsjers in 2018:studie
Jaar van extremen voor krimpende Zwitserse gletsjers in 2018:studie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


