
Wetenschap
Bondstypen begrijpen:de rol van elektronegativiteit
1. Het verschil in elektronegativiteit:
* Ionische bindingen: Wanneer het elektronegativiteitsverschil tussen twee atomen groot is (doorgaans groter dan 1,7), zal het atoom met een hogere elektronegativiteit effectief het elektron (de elektronen) van het minder elektronegatieve atoom "stelen". Dit resulteert in de vorming van ionen (positief en negatief geladen atomen) en een elektrostatische aantrekkingskracht daartussen, waardoor een ionische binding ontstaat.
* Covalente obligaties: Wanneer het elektronegativiteitsverschil klein is (doorgaans minder dan 1,7), delen de atomen elektronen om een stabiele elektronenconfiguratie te bereiken. Dit delen vormt een covalente band.
2. Soorten covalente obligaties:
* Niet-polaire covalente obligaties: Wanneer het elektronegativiteitsverschil erg klein is (bijna nul), worden de elektronen gelijkelijk verdeeld tussen de twee atomen. Dit resulteert in een niet-polaire covalente binding.
* Polaire covalente obligaties: Wanneer het elektronegativiteitsverschil gematigd is (tussen 0,5 en 1,7), worden de elektronen ongelijk verdeeld. Het atoom met een hogere elektronegativiteit zal de gedeelde elektronen sterker aantrekken, wat resulteert in een licht negatieve lading op dat atoom en een licht positieve lading op het andere. Hierdoor ontstaat een polaire covalente binding met een dipoolmoment.
Belangrijkste punten om te onthouden:
* Elektronegativiteit is een relatieve eigenschap. Het vertelt je niet de absolute "aantrekkingskracht" op elektronen, maar eerder hoe sterk een atoom elektronen aantrekt in vergelijking met een ander atoom.
* Hoe groter het elektronegativiteitsverschil, hoe ionischer de binding.
* Hoe kleiner het elektronegativiteitsverschil, hoe covalenter de binding.
* Elektronegativiteitswaarden worden gegeven op een schaal (bijvoorbeeld de Pauling-schaal). U kunt deze waarden gebruiken om het elektronegativiteitsverschil tussen twee atomen te berekenen.
Voorbeeld:
* NaCl (natriumchloride): Natrium (Na) heeft een elektronegativiteit van 0,93, terwijl chloor (Cl) een elektronegativiteit van 3,16 heeft. Het verschil is 2,23, wat wijst op een groot elektronegativiteitsverschil. Daarom vormt NaCl een ionische binding.
* H₂O (water): Zuurstof (O) heeft een elektronegativiteit van 3,44, terwijl waterstof (H) een elektronegativiteit van 2,20 heeft. Het verschil is 1,24, wat wijst op een matig elektronegativiteitsverschil. Daarom vormt H₂O polaire covalente bindingen.
* H₂ (waterstof): Beide waterstofatomen hebben dezelfde elektronegativiteit (2,20). Het elektronegativiteitsverschil is nul, wat leidt tot een niet-polaire covalente binding.
Samenvattend bieden verschillen in elektronegativiteit een waardevol hulpmiddel voor het voorspellen van het type binding dat zich tussen twee atomen zal vormen, en bieden ze inzicht in de aard en het gedrag van moleculen.
 Dragende verstrikkingen in polymeerglazen
Dragende verstrikkingen in polymeerglazen Wat is het verschil tussen watervrije ammoniak en aqua-ammoniak?
Wat is het verschil tussen watervrije ammoniak en aqua-ammoniak?  Biovriendelijke protocellen pompen bloedvaten op
Biovriendelijke protocellen pompen bloedvaten op Wat is de geschatte vriespuntdepressie van 0,020 m waterige NABR -oplossing?
Wat is de geschatte vriespuntdepressie van 0,020 m waterige NABR -oplossing?  Het benoemen van organische verbindingen:wat is de IUPAC-naam voor CH3CHFC2H5?
Het benoemen van organische verbindingen:wat is de IUPAC-naam voor CH3CHFC2H5?
 Expeditie Papoea-Nieuw-Guinea ontdekt grootste bomen op extreme hoogte
Expeditie Papoea-Nieuw-Guinea ontdekt grootste bomen op extreme hoogte Hete rotsen, geen warme sfeer, leidde tot relatief recente door water uitgesleten valleien op Mars
Hete rotsen, geen warme sfeer, leidde tot relatief recente door water uitgesleten valleien op Mars Verschillende bronnen van water
Verschillende bronnen van water Bewijs opgraven:onderzoekers onderzoeken processen die bodemgezondheid ondersteunen
Bewijs opgraven:onderzoekers onderzoeken processen die bodemgezondheid ondersteunen Wat leeft in het water maar wordt nooit nat?
Wat leeft in het water maar wordt nooit nat?
Hoofdlijnen
- Onderzoek bevestigt dat identiteitsverwisseling kan verklaren waarom haaien mensen bijten
- Wat is de juiste naam voor een systeem van wortels die groeit als één grote verticale wortel met kleinere laterale uitlopers?
- Wat is superieur DNA?
- Is de t rex een prokaryote of eukaryote -cel?
- Wat gebeurt er als een cel geen Golgi -apparaat heeft?
- Wat is de dunne laag van scheidingscellen genoemd die verantwoordelijk zijn voor groei?
- Wat zijn de vier steriele sites in het menselijk lichaam?
- Verschillen tussen Protista en Monera
- Wat is een vivovore?
- Nieuwe methode ontdekt om eiwitten in menselijke cellen te bekijken
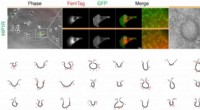
- Ingenieurs maken injecteerbare weefsels werkelijkheid

- Biocompatibele hydrogelmaterialen kunnen snel herstellen van mechanische stress
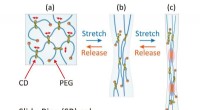
- Krachtcentrales aangedreven door licht

- Kleine belletjes op elektroden zijn essentieel voor het versnellen van chemische processen

 Wat zijn de ingangen en uitgangen van cellulaire ademhaling?
Wat zijn de ingangen en uitgangen van cellulaire ademhaling?  Minder vooringenomen gezichtsherkenning? Microsoft prijst verbetering, IBM biedt hulp
Minder vooringenomen gezichtsherkenning? Microsoft prijst verbetering, IBM biedt hulp Verschillen tussen Borax en Borateem
Verschillen tussen Borax en Borateem  Wat is een ander woord dat wetenschappers fouten gebruiken?
Wat is een ander woord dat wetenschappers fouten gebruiken?  Wat is het orbitale diagram voor 24 cr?
Wat is het orbitale diagram voor 24 cr?  Wat bedekt het licht van een microscoop om de golflengte te verkorten?
Wat bedekt het licht van een microscoop om de golflengte te verkorten?  Stijgende temperaturen verlagen de relatieve vochtigheid:waarom het ertoe doet
Stijgende temperaturen verlagen de relatieve vochtigheid:waarom het ertoe doet  Biocomputer aangedreven door kwallen-DNA speelt Tetris en andere retro-videogames
Biocomputer aangedreven door kwallen-DNA speelt Tetris en andere retro-videogames
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

