
Wetenschap
Elektronegativiteit en bindingspolariteit:chemische bindingen begrijpen
1. Elektronegativiteitsverschil en bindingspolariteit:
* Elektronegativiteit is het vermogen van een atoom in een molecuul om elektronen naar zich toe te trekken.
* Hoe groter het elektronegativiteitsverschil tussen twee atomen, hoe meer polair de band. Dit betekent dat de elektronen ongelijk verdeeld zijn, waardoor ze meer tijd doorbrengen in de buurt van het meer elektronegatieve atoom.
2. Soorten obligaties gebaseerd op elektronegativiteit:
* Niet-polaire covalente obligaties: Wanneer het elektronegativiteitsverschil tussen twee atomen erg klein is (doorgaans minder dan 0,5), worden de elektronen vrijwel gelijk verdeeld. Dit resulteert in een niet-polaire covalente binding .
* Polaire covalente obligaties: Wanneer het elektronegativiteitsverschil gematigd is (tussen 0,5 en 1,7), worden de elektronen ongelijk verdeeld. Hierdoor ontstaat een polaire covalente binding met gedeeltelijk positieve en gedeeltelijk negatieve ladingen op de atomen.
* Ionische bindingen: Wanneer het elektronegativiteitsverschil groot is (meestal groter dan 1,7), *neemt* het ene atoom effectief het elektron van het andere. Hierdoor ontstaan ionen met volledige positieve en negatieve lading, wat leidt tot een ionbinding .
3. Gevolgen van bindingspolariteit:
* Moleculaire dipoolmomenten: Polaire covalente bindingen creëren een dipoolmoment in een molecuul, wat betekent dat het molecuul een positief en een negatief uiteinde heeft. Dit beïnvloedt de interactie van het molecuul met andere moleculen en zijn algehele gedrag.
* Oplosbaarheid: Polaire moleculen hebben de neiging op te lossen in polaire oplosmiddelen, terwijl niet-polaire moleculen oplossen in niet-polaire oplosmiddelen.
* Chemische reactiviteit: Bondpolariteit beïnvloedt de reactiviteit van moleculen. Het is bijvoorbeeld waarschijnlijker dat polaire moleculen deelnemen aan reacties waarbij ladingsinteracties betrokken zijn.
Samengevat:
Het verschil in elektronegativiteit dicteert rechtstreeks het karakter van een binding. Dit bepaalt het delen van elektronen, creëert bindingspolariteit en beïnvloedt de algemene eigenschappen en reactiviteit van moleculen.
 Hoe wordt het spirituele pad in het hindoeïsme genoemd?
Hoe wordt het spirituele pad in het hindoeïsme genoemd?  Waarom zou een wetenschapper geïnteresseerd kunnen zijn in de regenwouden?
Waarom zou een wetenschapper geïnteresseerd kunnen zijn in de regenwouden?  Studie onthult mechanismen die ijsvorming bevorderen die verantwoordelijk zijn voor stroomonderbrekingen
Studie onthult mechanismen die ijsvorming bevorderen die verantwoordelijk zijn voor stroomonderbrekingen Bosduff moet worden overwogen bij gecontroleerde verbranding om schade aan bomen te voorkomen
Bosduff moet worden overwogen bij gecontroleerde verbranding om schade aan bomen te voorkomen Waarom is het belangrijk om alle natuurlijke hulpbronnen zorgvuldig te gebruiken?
Waarom is het belangrijk om alle natuurlijke hulpbronnen zorgvuldig te gebruiken?
Hoofdlijnen
- Wat is de AdvangTage van Asextaul -reproductie?
- Bijenvival:herstelt de bijenpopulatie in Texas zich?
- Wat is de functie van enzymen in planten?
- Wat is het belang van het bestuderen van cellenstructuur?
- Wat zijn de niveaus van biologische classificatie van grootste groepering tot kleinste groepering?
- Telt de menselijke mond als orgaan?
- Reproduceren zeer weinig cellen een van de principesceltheorie?
- Type classificatie op basis van evolutionaire geschiedenis?
- Waar gaan microplastics naar de oceanen?
- De zon vangen:nieuwe dunnefilmtechnologie maakt gebruik van duurzame componenten voor zonnepanelen

- Spinpeptiden bestrijden superbacteriën en kanker
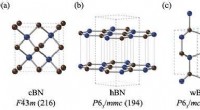
- De meest stabiele boornitridestructuur voorspellen met kwantumsimulaties
- Gesmolten staal monitoren met laser – uitvinding van staalexperts kan de industrie miljoenen besparen

- Betere chemie door kleine antennes

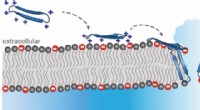
 Men denkt dat de extracellulaire matrix deelneemt aan de regulering van het gedrag van dierenoproep door informatie van buiten in de cel te communiceren via?
Men denkt dat de extracellulaire matrix deelneemt aan de regulering van het gedrag van dierenoproep door informatie van buiten in de cel te communiceren via?  Hoe biedt HIV een echtmodel van evolutie?
Hoe biedt HIV een echtmodel van evolutie?  In een enorm gebied in de ruimte, astronomen vinden veel minder sterrenstelsels dan ze hadden verwacht
In een enorm gebied in de ruimte, astronomen vinden veel minder sterrenstelsels dan ze hadden verwacht Wat zijn de pinakels in zwan?
Wat zijn de pinakels in zwan?  Ubuntu biedt lessen over de behandeling van mensen met een handicap:een onderzoek naar Bomvana-rituelen
Ubuntu biedt lessen over de behandeling van mensen met een handicap:een onderzoek naar Bomvana-rituelen  Onderzoekers verkennen nieuw hoofdstuk in de natuurkunde
Onderzoekers verkennen nieuw hoofdstuk in de natuurkunde Wat gebeurt er met een pathogene schimmel die in de ruimte groeit?
Wat gebeurt er met een pathogene schimmel die in de ruimte groeit?  Wat is het verschil tussen epidermis van menselijke en ongewervelde dieren?
Wat is het verschil tussen epidermis van menselijke en ongewervelde dieren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

