
Wetenschap
Berekening van het aantal koolstofmoleculen voor hematietreactie:een stapsgewijze handleiding
1. Schrijf de uitgebalanceerde chemische vergelijking:
Bij de reactie tussen koolstof (C) en hematiet (Fe₂O₃) ontstaat ijzer (Fe) en kooldioxide (CO₂):
2 Fe₂O₃ + 3 C → 4 Fe + 3 CO₂
2. Bereken het aantal mol hematiet:
* Zoek de molaire massa van hematiet (Fe₂O₃):(2 * 55,845 g/mol Fe) + (3 * 16,00 g/mol O) =159,69 g/mol
* Deel de massa van hematiet door zijn molaire massa:580 g / 159,69 g/mol =3,63 mol Fe₂O₃
3. Bepaal de molverhouding uit de uitgebalanceerde vergelijking:
* Uit de uitgebalanceerde vergelijking blijkt dat 3 mol koolstof reageert met 2 mol hematiet.
4. Bereken het aantal benodigde mol koolstof:
* Stel een verhouding in:(3 mol C / 2 mol Fe₂O₃) =(x mol C / 3,63 mol Fe₂O₃)
* Los op voor x:x =(3 mol C * 3,63 mol Fe₂O₃) / 2 mol Fe₂O₃ =5,45 mol C
Je hebt dus 5,45 mol koolstof nodig om te reageren met 580 g hematiet.
 Van spiegelbeeldbiologie tot verbeterde therapeutische eiwitten
Van spiegelbeeldbiologie tot verbeterde therapeutische eiwitten Welk element komt voor als geel poeder?
Welk element komt voor als geel poeder?  RNA-streng maakt het vangen van uracil in de kritieke toestand mogelijk
RNA-streng maakt het vangen van uracil in de kritieke toestand mogelijk Van welke laag wordt aangenomen dat het zich het meest als een vloeistof gedraagt?
Van welke laag wordt aangenomen dat het zich het meest als een vloeistof gedraagt?  Welk experiment overtuigde Ernest Rutherford dat het atoom een kleine positiviteitskleur heeft?
Welk experiment overtuigde Ernest Rutherford dat het atoom een kleine positiviteitskleur heeft?
 Noordse landen roepen op tot wereldwijd verdrag tegen plasticvervuiling in de oceaan
Noordse landen roepen op tot wereldwijd verdrag tegen plasticvervuiling in de oceaan Waarom heb je wetenschap in je leven nodig?
Waarom heb je wetenschap in je leven nodig?  Aanjager van de grootste massa-extinctie in de geschiedenis van de aarde geïdentificeerd
Aanjager van de grootste massa-extinctie in de geschiedenis van de aarde geïdentificeerd Hoewel tropische regenwouden rijke vegetatie hebben, zijn de natuurlijke omstandigheden niet gunstig voor de landbouw?
Hoewel tropische regenwouden rijke vegetatie hebben, zijn de natuurlijke omstandigheden niet gunstig voor de landbouw?  Klimaatverandering veroorzaakte de verwoestende overstromingen in een deel van het zuidoosten van Brazilië, studie zegt:
Klimaatverandering veroorzaakte de verwoestende overstromingen in een deel van het zuidoosten van Brazilië, studie zegt:
Hoofdlijnen
- Bij dieren is welk stadium welk stage dominanter haploïde of diploïde?
- UW-wetenschappers ontrafelen het mysterie van hoe griepvirussen zich vermenigvuldigen
- Genetische barcodes worden gebruikt om cruciale populaties in een ecosysteem van koraalriffen te kwantificeren
- Verandert de ploid van een cel wanneer deze door mitose verdeelt waarom of waarom niet?
- Primatengif werpt licht op waarom zoveel mensen last hebben van kattenallergieën
- Wat is het verschil tussen bioleaching en fytomining?
- Plasticity Cell Definition
- Probiotische combinatie verbetert de overleving van oesterlarven drastisch
- Hoeveel nucleotiden zitten er in één triplet?
- Een methode voor computerondersteunde modellering en simulatie van grote eiwitten en andere biomoleculen

- Nieuwe solid-state thermische diode ontwikkeld met betere rectificatieprestaties

- Wetenschappers ontwikkelen supergevoelige sensoren voor spiegelmoleculen in medicijnen
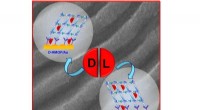
- Moleculaire dispersie verbetert quasi-dubbellaagse organische zonnecellen

- Berekening van de pH van een ammoniakoplossing met behulp van de base-dissociatieconstante (Kb)

 Welk element heeft een massaal nummer van 27?
Welk element heeft een massaal nummer van 27?  De maan is de perfecte plek voor SETI
De maan is de perfecte plek voor SETI Wat zijn de drie soorten vaste neerslag?
Wat zijn de drie soorten vaste neerslag?  Wetenschapsexperimenten met Prisms
Wetenschapsexperimenten met Prisms Welk enzym functioneert in zeer zure omstandigheden?
Welk enzym functioneert in zeer zure omstandigheden?  Kernenergieprogramma's vergroten de kans op proliferatie niet, studie vondsten
Kernenergieprogramma's vergroten de kans op proliferatie niet, studie vondsten Is de zon net door de wolken heen gebroken?
Is de zon net door de wolken heen gebroken?  Orkaan Fiona laat een dode achter in de Dominicaanse Republiek na verwoesting van Puerto Rico
Orkaan Fiona laat een dode achter in de Dominicaanse Republiek na verwoesting van Puerto Rico
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

