
Wetenschap
Xenon-reactiviteit:de uitzondering op edelgas begrijpen
Xenon is echter niet geheel onreactief . Onder bepaalde omstandigheden kan het verbindingen vormen, met name met zeer elektronegatieve elementen zoals fluor en zuurstof. Deze verbindingen worden over het algemeen als zeer onstabiel beschouwd en vereisen dat er specifieke voorwaarden ontstaan.
Hier is een overzicht van de reactiviteit van xenon:
* Normale omstandigheden: Xenon is uiterst reactief en vormt niet gemakkelijk verbindingen.
* Extreme omstandigheden:
* Hoge druk en temperatuur: Kan leiden tot de vorming van verbindingen zoals XeF2 , XeF4 , en XeO3 .
* Aanwezigheid van sterke oxidatiemiddelen: Deze kunnen reageren met xenon en zo verbindingen vormen zoals XeO2 en XeO4 .
Voorbeelden van xenonverbindingen:
* Xenondifluoride (XeF2 ): Een kleurloze vaste stof, gebruikt in sommige lasertoepassingen.
* Xenon-tetrafluoride (XeF4 ): Een witte vaste stof, gebruikt bij de synthese van andere xenonverbindingen.
* Xenonhexafluoride (XeF6 ): Een kleurloos gas, gebruikt als fluoreringsmiddel.
Hoewel xenon wordt beschouwd als een edelgas en over het algemeen niet-reactief is, kan het onder specifieke omstandigheden verbindingen vormen. Deze reactiviteit, hoewel beperkt, heeft geleid tot interessante ontdekkingen en toepassingen op verschillende gebieden.
 Onderzoekers visualiseren de motor van bacteriën in de eerste stap naar door mensen geproduceerde elektrische energie
Onderzoekers visualiseren de motor van bacteriën in de eerste stap naar door mensen geproduceerde elektrische energie Waarom bepaalde ijsjes bestand zijn tegen smelten:een wetenschappelijke verklaring
Waarom bepaalde ijsjes bestand zijn tegen smelten:een wetenschappelijke verklaring  De evenwichtsconstante voor de onderstaande reactie is 0,625 bij O2 0,40 en H2O 0,20 Welke concentratie H2O2?
De evenwichtsconstante voor de onderstaande reactie is 0,625 bij O2 0,40 en H2O 0,20 Welke concentratie H2O2?  Wat zijn definities van mengsels?
Wat zijn definities van mengsels?  Wat bestaat uit slechts één atoom en heeft een chemisch symbool dat niet kan worden verdeeld in eenvoudiger stoffen?
Wat bestaat uit slechts één atoom en heeft een chemisch symbool dat niet kan worden verdeeld in eenvoudiger stoffen?
 Boomstammen van gemengde soorten passen zich beter aan dan pure stands
Boomstammen van gemengde soorten passen zich beter aan dan pure stands Vleermuizen hangen waar ooit Israëlische soldaten stonden in de Jordaanvallei
Vleermuizen hangen waar ooit Israëlische soldaten stonden in de Jordaanvallei Planten zijn afhankelijk van de atmosfeer als grootste bron van?
Planten zijn afhankelijk van de atmosfeer als grootste bron van?  Bodembiologisch onderzoek kan bijdragen aan een duurzamere toekomst
Bodembiologisch onderzoek kan bijdragen aan een duurzamere toekomst Onderzoek toont aan dat lozing van giftige mijnen het Blue Mountains-werelderfgoedgebied binnenstroomt
Onderzoek toont aan dat lozing van giftige mijnen het Blue Mountains-werelderfgoedgebied binnenstroomt
Hoofdlijnen
- Onderzoekers werpen licht op hoe een belangrijk ingrediënt voor leven zich in de ruimte kan vormen
- Waar geven endocriene klieren chemicaliën vrij?
- Welke organismen gebruiken cellulaire ademhaling?
- Welk complex van twee eiwitten geeft het OK -signaal voor een cel om te beginnen met mitose?
- Hadden dinosaurussen veren?
- Methanotrofen:kunnen bacteriën ons milieu helpen beschermen?
- Kunnen honden snel woorden leren?
- Welk wetenschappelijk hulpmiddel is uitgevonden om wetenschappers te helpen heel kleine dingen zoals bacteriën te zien?
- Wat is de pH van menselijk orgaan?
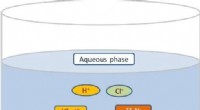
- Het mechanisme van metaalextractie met ionische vloeistoffen bestuderen
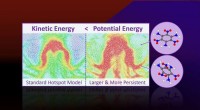
- Onderzoek onthult ontbrekende fysica in explosieve hotspots
- Onderzoek naar de deeltjesgrootte en depositie van dampen

- Hightech oppervlakken kunnen de weerstand en CO2-uitstoot van schepen aanzienlijk verminderen

- Nieuwe toepassingen vinden voor afvalbanden

 Hoe verbeteren biometrische apparaten de beveiliging?
Hoe verbeteren biometrische apparaten de beveiliging?  Welke sfeer maken mensen deel uit?
Welke sfeer maken mensen deel uit?  Hoe hebben lichtstralen in de caleidoscoop om afbeelding te maken?
Hoe hebben lichtstralen in de caleidoscoop om afbeelding te maken?  Hoe Polar Bears Camouflage?
Hoe Polar Bears Camouflage?  Zwarte mannen worden geconfronteerd met hoge discriminatie en depressie, zelfs als hun opleiding en inkomen stijgen
Zwarte mannen worden geconfronteerd met hoge discriminatie en depressie, zelfs als hun opleiding en inkomen stijgen Wat is het doel van een spoel in een luidspreker?
Wat is het doel van een spoel in een luidspreker?  Kooldioxidemineralisatie in geologisch veel voorkomende gesteenten voor koolstofopslag
Kooldioxidemineralisatie in geologisch veel voorkomende gesteenten voor koolstofopslag Chemische gevarensymbolen begrijpen:OSHA- en NFPA-richtlijnen
Chemische gevarensymbolen begrijpen:OSHA- en NFPA-richtlijnen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

