
Wetenschap
Overgangsmetalen:gemeenschappelijke ionenladingen en variabele oxidatietoestanden
* Variabele oxidatietoestanden: Overgangsmetalen hebben meerdere elektronen in hun d-orbitalen, die betrokken zijn bij binding. Hierdoor kunnen ze verschillende aantallen elektronen verliezen, wat resulteert in verschillende oxidatietoestanden (positieve ladingen).
* Gemeenschappelijke oxidatietoestanden: Hoewel ze verschillende oxidatietoestanden kunnen hebben, komen sommige vaker voor dan andere. De gebruikelijke oxidatietoestanden voor ijzer (Fe) zijn bijvoorbeeld +2 en +3, terwijl koper (Cu) vaak +1 en +2 heeft.
Belangrijke opmerking: De specifieke lading van een overgangsmetaalion hangt af van het element en de chemische omgeving waarin het zich bevindt.
Laat het me weten als je voorbeelden wilt van specifieke overgangsmetalen en hun gemeenschappelijke ionen!
 Wat is de naam voor chemische boodschappers?
Wat is de naam voor chemische boodschappers?  Bacteriën als levende fabrieken voor de productie van krachtige antibiotica
Bacteriën als levende fabrieken voor de productie van krachtige antibiotica Wat is een polair molecuul dat lichte negatieve lading in de buurt van het element heeft?
Wat is een polair molecuul dat lichte negatieve lading in de buurt van het element heeft?  Wat beschrijft de definitie van atomaire massa het beste een element?
Wat beschrijft de definitie van atomaire massa het beste een element?  Wat is de natuurlijke bron van chloor?
Wat is de natuurlijke bron van chloor?
 Nieuw onderzoek kan de droogte van La Nina jaren van tevoren voorspellen
Nieuw onderzoek kan de droogte van La Nina jaren van tevoren voorspellen Langetermijngegevens laten een recente versnelling zien in chemische en fysische veranderingen in de oceaan
Langetermijngegevens laten een recente versnelling zien in chemische en fysische veranderingen in de oceaan Wereldwijde gemeenschap komt bijeen voor het rif
Wereldwijde gemeenschap komt bijeen voor het rif Onderzoekers lossen het vormingsmechanisme van sferische carbonaatconcreties op
Onderzoekers lossen het vormingsmechanisme van sferische carbonaatconcreties op Studie onthult hoe grote droogtes in de Grotere Mekong leiden tot uitbarstingen van kooldioxide-emissies
Studie onthult hoe grote droogtes in de Grotere Mekong leiden tot uitbarstingen van kooldioxide-emissies
Hoofdlijnen
- GoT-ChA:Nieuw hulpmiddel onthult hoe genmutaties cellen beïnvloeden
- Normale menselijke genen overbrengen naar cellen die ze missen, wordt ze genoemd?
- Welke structuur is vergelijkbaar met het endoplasmatische reticulum?
- Hoe vampieren werken
- Eerste video's die de helix van 'dansend DNA' laten zien, ontwikkeld door wetenschappers
- Het cytoplasma van een cel is?
- Wat is het proces waarbij stoffen de cellen binnenkomen en verlaten en binnen de cellen worden verdeeld?
- Hoe beïnvloeden zuren en basen een cellenomgeving?
- Ben jij de directe afstammelingen van een uitheemse soort?
- Een nieuwe manier om met zonlicht schone waterstofbrandstof te maken uit water

- Robotachtige zachte materie buigt, draait en kruipt wanneer geraakt met licht

- Het produceren van kunstmest uit lucht zou vijf keer zo efficiënt kunnen zijn
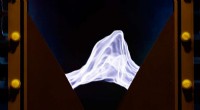
- Neutronen werpen licht op industriële katalysator voor waterstofproductie

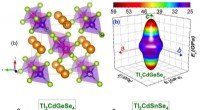
- Onderzoek naar nieuw gesynthetiseerde thalliumverbindingen voor opto-elektronische apparaten
 Kan verlichting stikstofverbindingen veranderen in gas?
Kan verlichting stikstofverbindingen veranderen in gas?  Hoe de speciale relativiteitstheorie werkt
Hoe de speciale relativiteitstheorie werkt  12 DM is gelijk aan hoeveel cm?
12 DM is gelijk aan hoeveel cm?  Wat is de energie van bewegende atomen?
Wat is de energie van bewegende atomen?  Wat is het belangrijkste effect van natriumhydroxide op eiwitten?
Wat is het belangrijkste effect van natriumhydroxide op eiwitten?  Wat gebeurt er als kinetische energie wordt omgezet in potentiële zwaartekrachtenergie?
Wat gebeurt er als kinetische energie wordt omgezet in potentiële zwaartekrachtenergie?  Wat verklaart het beste de relatie tussen ouderrots en bodemsamenstelling?
Wat verklaart het beste de relatie tussen ouderrots en bodemsamenstelling?  Je (kleine) bubbels laten barsten:nieuw onderzoek wijst de weg naar poriënvrij 3D-printen
Je (kleine) bubbels laten barsten:nieuw onderzoek wijst de weg naar poriënvrij 3D-printen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

