
Wetenschap
De stabiliteit van natrium:inzicht in de elektronenconfiguratie en de octetregel
* Elektronenconfiguratie: Natrium (Na) heeft 11 elektronen. De elektronenconfiguratie is 2, 8, 1. Dit betekent dat er één elektron in de buitenste schil (de derde schil) zit.
* Octetregel: De octetregel stelt dat atomen de neiging hebben elektronen te winnen, te verliezen of te delen om een stabiele configuratie van acht elektronen in hun buitenste schil te bereiken.
* Een elektron verliezen: Door zijn ene valentie-elektron te verliezen, wordt natrium een positief geladen ion (Na+). Hierdoor wordt het enkele elektron in de buitenste schil verwijderd, waardoor de elektronenconfiguratie 2, 8 overblijft, wat een volledige en stabiele tweede schil is.
Beschouw het als volgt:
Stel je de buitenste schil voor als een doos die acht knikkers kan bevatten. Natrium heeft slechts één knikker in zijn doos, waardoor deze instabiel is. Door die knikker kwijt te raken, wordt de doos geleegd en staat er nu een volle doos onder, wat een stabielere configuratie is.
Deze neiging om elektronen te verliezen en een stabiele configuratie te bereiken, is de drijvende kracht achter de reactiviteit van natrium en zijn vermogen om ionische bindingen met andere elementen te vormen.
Hoofdlijnen
- Welke wetenschappers hebben bijgedragen aan de evolutietheorie de studie van natuurlijke selectie?
- Welk macromolecuul is geslachtshormonen?
- Welk deel van de cel reguleert de ingang en uitgangsmoleculen voor cel?
- Welke weefsels bestaan uit cellen?
- Oude fossielen van reuzenschildpadden gevonden in de Colombiaanse Andes
- Wat is het directe resultaat van aerobe ademhaling?
- Wat zijn de beroepen in de levenswetenschap?
- P53 (TP53) Tumor Protein: Function, Mutation
- Hongerige berencrisis grijpt in het verre oosten van Rusland
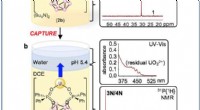
- Team ontwikkelt een elektrochemische methode om uranium te winnen, en mogelijk andere metaalionen, van oplossing
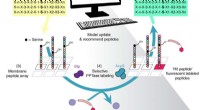
- Machine learning gebruiken om peptiden te ontwerpen
- Wetenschappers ontdekken bij toeval zeldzame clusterverbinding

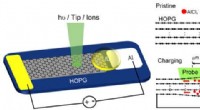
- Oppervlakte-effect van elektroden onthuld door operando oppervlaktewetenschapsmethodologie
- Nieuwe verbinding effectief tegen medicijnresistente pathogenen, kan leiden tot nieuwe antibiotica

 Energieproductie vindt plaats in het A endoplasmatisch reticulum B Chloroplast C Mitochondria D Ribosoom?
Energieproductie vindt plaats in het A endoplasmatisch reticulum B Chloroplast C Mitochondria D Ribosoom?  Onderzoekers ontwikkelen systeem voor vroegtijdige waarschuwing om online desinformatie te bestrijden
Onderzoekers ontwikkelen systeem voor vroegtijdige waarschuwing om online desinformatie te bestrijden Bestrijdingsmiddelenmengsels groter probleem dan eerder gedacht
Bestrijdingsmiddelenmengsels groter probleem dan eerder gedacht De huidige toezeggingen om steenkoolstroom uit te faseren zijn kritisch onvoldoende om de klimaatverandering te vertragen
De huidige toezeggingen om steenkoolstroom uit te faseren zijn kritisch onvoldoende om de klimaatverandering te vertragen Vulkanen die in de laatste 100 jaar zijn gebroken
Vulkanen die in de laatste 100 jaar zijn gebroken  Wanneer twee krachten zijn wat er een verandering in positie of beweging is?
Wanneer twee krachten zijn wat er een verandering in positie of beweging is?  Het installeren van zonnepanelen op landbouwgronden maximaliseert hun efficiëntie, nieuwe studie toont
Het installeren van zonnepanelen op landbouwgronden maximaliseert hun efficiëntie, nieuwe studie toont Hoe zijn slakken gerelateerd aan de milieuwetenschap?
Hoe zijn slakken gerelateerd aan de milieuwetenschap?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


