
Wetenschap
Inzicht in de zuurgraad van zoutzuur (HCl)
1. Protonen (H+) donatie:
* HCl dissocieert gemakkelijk in water, waarbij een waterstofion (H+) en een chloride-ion (Cl-) vrijkomen:
* HCl (aq) → H+ (aq) + Cl- (aq)
*Het vermogen om een proton (H+) te doneren is het bepalende kenmerk van een zuur, volgens de zuur-base-theorie van Brønsted-Lowry.
2. pH:
* Waterige oplossingen van HCl hebben een pH van minder dan 7, wat wijst op hun zure aard. Hoe lager de pH, hoe sterker het zuur.
3. Reactie met basen:
* HCl reageert met basen (zoals NaOH) en vormt zout (NaCl) en water (H2O):
* HCl (water) + NaOH (water) → NaCl (water) + H2O (l)
* Deze neutralisatiereactie is kenmerkend voor zuren.
4. Aanwezigheid van waterstofionen:
* De aanwezigheid van een waterstofion (H+) in de structuur, dat gemakkelijk kan dissociëren, draagt bij aan de zure aard van HCl.
5. Elektronenacceptor:
*Volgens de Lewis-zuur-base-theorie is een zuur een elektronenacceptor. HCl kan een elektronenpaar accepteren, waardoor het een zuur wordt.
Samenvattend dragen het vermogen van HCl om protonen te doneren, de lage pH, de reactie met basen en de aanwezigheid van een waterstofion in de structuur allemaal bij aan de classificatie ervan als zuur.
 Nieuw materiaal maakt koelapparaten energiezuiniger
Nieuw materiaal maakt koelapparaten energiezuiniger Video:De chemie achter zwart poeder
Video:De chemie achter zwart poeder Welke kleur is bismut?
Welke kleur is bismut?  Wetenschappers gebruiken een blender om te onthullen wat er in onze smartphones zit
Wetenschappers gebruiken een blender om te onthullen wat er in onze smartphones zit Onderzoek onthult de migratieroute in de gasfase voor de vorming van een sterke interactietoestand tussen metaal en drager
Onderzoek onthult de migratieroute in de gasfase voor de vorming van een sterke interactietoestand tussen metaal en drager
 NASA-NOAA satellietbeelden 's nachts volgen tropische depressie Laura boven de VS
NASA-NOAA satellietbeelden 's nachts volgen tropische depressie Laura boven de VS Zeevogelnesten zitten vol met weggegooid plastic afval
Zeevogelnesten zitten vol met weggegooid plastic afval Californië verplicht 100 procent emissievrije busvloot
Californië verplicht 100 procent emissievrije busvloot Wat is een natuurramp voor kinderen?
Wat is een natuurramp voor kinderen?  Veranderingen veroorzaakt door verergerende bosbranden in Californische bossen zullen eeuwen duren
Veranderingen veroorzaakt door verergerende bosbranden in Californische bossen zullen eeuwen duren
Hoofdlijnen
- De studie van het menselijk lichaam is welke wetenschap?
- Wat biedt de cel structurele ondersteuning?
- Vergelijking van vier methoden voor de droogefficiëntie en fysisch-chemische eigenschappen van kippenvlees
- Wat maakt mensen menselijk?
- Welke observatie bewijst dat cel Eurkaryote is?
- Waarom hebben spiercellen meer mitochondriën dan enig ander celtype?
- Welk type gen heeft identieke allelen?
- Wat betekent het voor soorten om een evolutionaire relatie te hebben?
- Wat is botfysiologie?
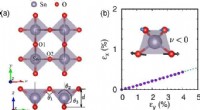
- Onderzoekers maken theoretische voorspelling van 2-D halfgeleider tindioxide
- VCU-uitvinders handapparaat brengt enorme verbeteringen aan het watertestproces

- Nieuw proces kan 3D-geprinte materialen met 200 procent versterken

- Studie onthult dynamisch gedrag van Cu-N-C-katalysator met één atoom in elektrokatalyse

- Onderzoek toont aan dat het doen van de twist hot is, ontspannen is cool

 Wat betekent Jupiter?
Wat betekent Jupiter?  Een openbaar toilet doorspoelen? blijf niet hangen, omdat aerosoldruppels dat wel doen
Een openbaar toilet doorspoelen? blijf niet hangen, omdat aerosoldruppels dat wel doen Hoe druk de platentektoniek aandrijft
Hoe druk de platentektoniek aandrijft  Kunnen twee auto's met dezelfde snelheid bewegen?
Kunnen twee auto's met dezelfde snelheid bewegen?  Wat zou er gebeuren met deze streng DNA tijdens transcriptie TACGCGCATTGTCGTCTAGGTTTCGATATATTAGCTACG?
Wat zou er gebeuren met deze streng DNA tijdens transcriptie TACGCGCATTGTCGTCTAGGTTTCGATATATTAGCTACG?  Een object gemaakt van rots of metaal dat de zon?
Een object gemaakt van rots of metaal dat de zon?  High-tech tools onthullen opalen fossiel skelet
High-tech tools onthullen opalen fossiel skelet De regen en overstromingen van orkaan Barry's hameren op de omgeving van de Golf
De regen en overstromingen van orkaan Barry's hameren op de omgeving van de Golf
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

