
Wetenschap
CH3Li Bond-karakter:ionisch versus covalent - Inzicht in de hybride aard
Dit is waarom:
* Verschil in elektronegativiteit: Het elektronegativiteitsverschil tussen koolstof (2,55) en lithium (0,98) is relatief groot (1,57). Dit suggereert dat de binding polair zou zijn, waarbij lithium een gedeeltelijk positieve lading draagt en koolstof een gedeeltelijk negatieve lading.
* De metaalachtige aard van lithium: Lithium is een zeer elektropositief element, wat betekent dat het gemakkelijk zijn elektron verliest en een positief ion (Li+) vormt.
* Structuur: De structuur van CH3Li suggereert een ionisch karakter. Het bestaat als een polymere structuur waarin lithiumionen zijn gecoördineerd met koolstofatomen.
* Reactiviteit: CH3Li is een sterke base en nucleofiel. De reactiviteit ervan komt overeen met de aanwezigheid van een zeer polaire of ionische binding.
De binding tussen koolstof en lithium in CH3Li heeft echter ook een covalent karakter vanwege:
* Elektronen delen: Hoewel de binding voornamelijk ionisch is, is er een zekere mate van elektronendeling tussen koolstof en lithium.
* Verbindingssterkte: De binding is relatief sterk, wat doorgaans niet wordt waargenomen bij puur ionische bindingen.
Daarom kan CH3Li het best worden omschreven als een ionische verbinding met een significant covalent karakter.
 Gebruik maken van de zon om vers water te brengen naar afgelegen of door rampen getroffen gemeenschappen
Gebruik maken van de zon om vers water te brengen naar afgelegen of door rampen getroffen gemeenschappen Onderzoek wijst op ethische inkoop van materialen voor moderne technologie
Onderzoek wijst op ethische inkoop van materialen voor moderne technologie Bereken het aantal ATP's dat is gegenereerd uit één verzadigd 16-koolstofvetzuur veronderstellen dat elk NADH-molecuul 2,5 en FADH2 1,5 ATP's genereert?
Bereken het aantal ATP's dat is gegenereerd uit één verzadigd 16-koolstofvetzuur veronderstellen dat elk NADH-molecuul 2,5 en FADH2 1,5 ATP's genereert?  Wat gebeurt er wanneer een basis wordt toegevoegd aan een bufferoplossing?
Wat gebeurt er wanneer een basis wordt toegevoegd aan een bufferoplossing?  Welke voedingsstof is het nodig in grote hoeveelheden?
Welke voedingsstof is het nodig in grote hoeveelheden?
 Is vleesvrij eten het antwoord op klimaatverandering?
Is vleesvrij eten het antwoord op klimaatverandering? Pennsylvania correleert aardgasfractie met aardbevingen
Pennsylvania correleert aardgasfractie met aardbevingen Op welke sfeer leven we?
Op welke sfeer leven we?  Ozonafbrekende stoffen veroorzaakten de helft van de opwarming van het noordpoolgebied in de late 20e eeuw. zegt studie
Ozonafbrekende stoffen veroorzaakten de helft van de opwarming van het noordpoolgebied in de late 20e eeuw. zegt studie Digitale ruimte vervangt de openbare ruimte niet, en misschien zelfs helpen om het beter te maken
Digitale ruimte vervangt de openbare ruimte niet, en misschien zelfs helpen om het beter te maken
Hoofdlijnen
- Wat bevat genetisch materiaal van een eukaryotische cel?
- Wat zijn roofdieren prooi parasieten fotosynthetische producenten en andere organismen die worden genoemd?
- Onkruidrijst is herbicideresistent geworden door snelle evolutie
- Waar worden aseksuele sporen gevormd?
- Welke wetenschapper bestuderen organismen en hun omgeving?
- Wat is de unieke betekenis van letters a g t en c voor biologen?
- Hoe werken de organellen in een cel samen?
- Hoeveel allels per gen zijn er in elke fase van meiose?
- Wat is de pH in speeksel?
- Ionen gevormd wanneer zilvernitraat oplost in water

- Nieuw membraanwaterbehandelingssysteem om giftig afval en afvalverwerkingskosten met meer dan 90 procent te verminderen

- Vogelveren inspireren onderzoekers om levendige nieuwe kleuren te produceren

- Goedkoop, energiezuinige aanpak voor de behandeling van met zware metalen verontreinigd water

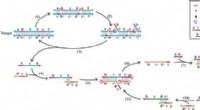
- Eenvoudig kopiëren:een universele isotherme DNA-amplificatiemethode
 Wat zijn de voordelen en nadelen van het gebruik van magnetisch veld voor energie?
Wat zijn de voordelen en nadelen van het gebruik van magnetisch veld voor energie?  Wat zijn de structuren van ethylacetaat en hexaan?
Wat zijn de structuren van ethylacetaat en hexaan?  Hoe heet een negatieve versnelling?
Hoe heet een negatieve versnelling?  Hoe modificeren wetenschappers watermeloenen genetisch?
Hoe modificeren wetenschappers watermeloenen genetisch?  Fysieke waarden in de echte wereld hebben twee componenten?
Fysieke waarden in de echte wereld hebben twee componenten?  Twee identieke beelden worden buiten de ene geplaatst van kalksteen het andere graniet welk standbeeld zal het langzamer worden?
Twee identieke beelden worden buiten de ene geplaatst van kalksteen het andere graniet welk standbeeld zal het langzamer worden?  Welk transport vereist geen celsenergie?
Welk transport vereist geen celsenergie?  Hoe corrigerende lenzen werken
Hoe corrigerende lenzen werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

