
Wetenschap
Aluminiumsulfaat- en ammoniakreactie:de chemie begrijpen
De reactie begrijpen:
* Aluminiumsulfaat (Al₂(SO₄)₃): Dit is een oplosbaar zout dat in water dissocieert en aluminiumionen (Al³⁺) en sulfaationen (SO₄²⁻) vormt.
* Ammoniak (NH₃): Dit is een zwakke base die in water oplost en ammoniumionen (NH₄⁺) en hydroxide-ionen (OH⁻) vormt.
De reactie:
De reactie is een dubbele verplaatsingsreactie gevolgd door hydrolyse . Hier is een overzicht:
1. Eerste reactie:
Al₂(SO₄)₃(aq) + 6 NH₃(aq) + 6 H₂O(l) → 2 Al(OH)₃(s) + 3 (NH₄)₂SO₄(aq)
2. Uitleg:
* Aluminiumionen (Al³⁺) reageren met hydroxide-ionen (OH⁻) uit ammoniak en vormen aluminiumhydroxide (Al(OH)₃), wat een wit, gelatineus neerslag is.
* Ammoniumionen (NH₄⁺) combineren met sulfaationen (SO₄²⁻) en vormen ammoniumsulfaat ((NH₄)₂SO₄), dat opgelost blijft in de oplossing.
Belangrijke opmerkingen:
* Hydrolyse: Het aluminiumhydroxideneerslag is eigenlijk een product van hydrolyse. Wanneer Al³⁺-ionen in contact komen met water, reageren ze met watermoleculen om Al(OH)₃- en H⁺-ionen te vormen. Deze reactie wordt bevorderd door de aanwezigheid van ammoniak, dat H⁺-ionen verbruikt, waardoor de hydrolyse wordt bevorderd.
* pH-afhankelijkheid: De reactie is pH-afhankelijk. Bij een lagere pH (zuurder) is de kans kleiner dat de reactie optreedt. Bij een hogere pH (basischer) is de kans groter dat de reactie optreedt.
Algemeen:
De reactie tussen aluminiumsulfaat en ammoniak resulteert in de vorming van een wit aluminiumhydroxideneerslag en ammoniumsulfaat in oplossing. De reactie is een complex proces waarbij dubbele verdringing en hydrolyse betrokken zijn.
 Met deze techniek kunnen onderzoekers onderzoeken hoe materialen zich op atomair niveau binden
Met deze techniek kunnen onderzoekers onderzoeken hoe materialen zich op atomair niveau binden  Hoe wordt een zwavelatoom ion?
Hoe wordt een zwavelatoom ion?  Welke term wordt door chemicus gebruikt om kwantitatief een oplossing te beschrijven waarin relatief kleine hoeveelheid opgeloste oplossing oplost?
Welke term wordt door chemicus gebruikt om kwantitatief een oplossing te beschrijven waarin relatief kleine hoeveelheid opgeloste oplossing oplost?  Hoe het is anders a.m.u van koolstofisotopen?
Hoe het is anders a.m.u van koolstofisotopen?  Waarom worden bimetallische strips gebruikt in thermostaten?
Waarom worden bimetallische strips gebruikt in thermostaten?
 600 seismografen luisteren mee op de Alpen
600 seismografen luisteren mee op de Alpen Als een populatie van rupsen zich voedt met de bladerenbomen in het bos en voedsel voor vogels draait die ze opeten, welke aanpassing zou het meest waarschijnlijk evolueren?
Als een populatie van rupsen zich voedt met de bladerenbomen in het bos en voedsel voor vogels draait die ze opeten, welke aanpassing zou het meest waarschijnlijk evolueren?  Dieren die leven op gletsjers en ijsbergen
Dieren die leven op gletsjers en ijsbergen NASA ziet tropische storm Tembin-vorm
NASA ziet tropische storm Tembin-vorm Welke effecten hebben chloorfluorkoolstoffen op mensen?
Welke effecten hebben chloorfluorkoolstoffen op mensen?
Hoofdlijnen
- Hoe zijn cellen in multi-cellig organisme vergelijkbaar en verschillende cellen een enkel organisme?
- Rennen naar de wortels:bodemvocht beïnvloedt de snelheid van nematoden
- Wat is antimaterie en waarom doet het ertoe?
- Wat is cytokinese?
- Team ontwikkelt een efficiënt gastheer-vectorsysteem voor een modelarchaeon door op CRISPR gebaseerd gastheer-plasmide-conflict op te lossen
- Hoe omgaan dieren met de dieren?
- Wat te bestuderen voor IGCSE Biology Paper 6?
- Wat gebeurt er met het anaërobe organisme in aanwezigheid van zuurstof?
- Welke cellen hebben membraan gebonden oraganellen prokaryotisch of eukaryotisch?
- Bevroren koper gedraagt zich als edelmetaal in katalyse:studie

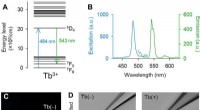
- Met terbium (III) gedoteerd fluorescerend glas voor biomedisch onderzoek
- Lab op een chip kan gezondheid monitoren, ziektekiemen en verontreinigende stoffen

- De interacties van chemische spiegelbeelden

- Gerichte evolutie opent deur naar nieuwe antibiotica
 Natures 3D-printer:Borstelwormen vormen stukje bij beetje borstelharen
Natures 3D-printer:Borstelwormen vormen stukje bij beetje borstelharen  Wat is de reden om perjoodzuur te noemen?
Wat is de reden om perjoodzuur te noemen?  Hoe valentie van radicalen te berekenen
Hoe valentie van radicalen te berekenen  Apple kent leverancier van glas voor iPhones $ 250 miljoen toe
Apple kent leverancier van glas voor iPhones $ 250 miljoen toe Oplossen voor specifieke zwaartekracht
Oplossen voor specifieke zwaartekracht  Landbeweging in Duitsland in kaart gebracht
Landbeweging in Duitsland in kaart gebracht De DNA -streng die niet wordt getranscribeerd, genaamd de streng.
De DNA -streng die niet wordt getranscribeerd, genaamd de streng.  Welk object kan briesje bewegen?
Welk object kan briesje bewegen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

