
Wetenschap
Ionische verbindingen:vorming, elementen en voorbeelden | Chemie uitgelegd
Hier is een overzicht:
* Metalen hebben de neiging elektronen te verliezen en kationen te vormen .
* Niet-metalen hebben de neiging elektronen te verkrijgen en anionen te vormen .
Belangrijkste elementen die ionische verbindingen vormen:
* Metalen: Groepen 1 (alkalimetalen), 2 (aardalkalimetalen), 3 (overgangsmetalen) en enkele elementen uit de groepen 13, 14 en 15.
* Niet-metalen: Groepen 16 (chalcogenen) en 17 (halogenen).
Voorbeelden:
* Natriumchloride (NaCl) :Natrium (Na) is een metaal in groep 1, en chloor (Cl) is een niet-metaal in groep 17. Natrium verliest één elektron om een kation te worden (Na+), terwijl chloor één elektron krijgt om een anion te worden (Cl-). Deze tegengesteld geladen ionen trekken elkaar aan en vormen de ionische verbinding NaCl.
* Magnesiumoxide (MgO) :Magnesium (Mg) is een metaal in groep 2, en zuurstof (O) is een niet-metaal in groep 16. Magnesium verliest twee elektronen om een kation te worden (Mg2+), terwijl zuurstof er twee elektronen bij krijgt om een anion te worden (O2-). Deze ionen trekken elkaar aan en vormen MgO.
Uitzonderingen:
* Ammoniumion (NH4+) is een polyatomair kation gevormd door de combinatie van stikstof en waterstof.
* Hydrooxide-ion (OH-) is een polyatomair anion gevormd door de combinatie van zuurstof en waterstof.
Samengevat:
Ionische verbindingen worden gevormd door de combinatie van elementen die gemakkelijk elektronen verliezen of winnen, wat resulteert in de vorming van positief en negatief geladen ionen die elkaar aantrekken als gevolg van elektrostatische krachten.
 Waarom wordt zout geclassificeerd als een mineraal?
Waarom wordt zout geclassificeerd als een mineraal?  Bereken het vries- en kookpunt van oplossingen:stapsgewijze handleiding
Bereken het vries- en kookpunt van oplossingen:stapsgewijze handleiding  Hoe maak je gloeiend water voor een Science Fair Project
Hoe maak je gloeiend water voor een Science Fair Project Mineralen die de elementen bevatten, worden silicium en zuurstof genoemd?
Mineralen die de elementen bevatten, worden silicium en zuurstof genoemd?  Team bereikt chemische reacties met twee elektronen met behulp van lichtenergie, goud
Team bereikt chemische reacties met twee elektronen met behulp van lichtenergie, goud
 Wat was speciaal aan Thorn Mountains National Forest?
Wat was speciaal aan Thorn Mountains National Forest?  Hoe kan het veranderende klimaat een beschaving beïnvloeden?
Hoe kan het veranderende klimaat een beschaving beïnvloeden? We weten dat het noordpoolgebied aan het opwarmen is:wat zullen veranderende rivierstromen met het milieu doen?
We weten dat het noordpoolgebied aan het opwarmen is:wat zullen veranderende rivierstromen met het milieu doen?  Waarom worden bladeren als materie beschouwd?
Waarom worden bladeren als materie beschouwd?  Observeren en experimenteren zijn twee manieren waarop ecologen wetenschappelijke vragen kunnen beantwoorden. Welke verschillen tussen deze benaderingen?
Observeren en experimenteren zijn twee manieren waarop ecologen wetenschappelijke vragen kunnen beantwoorden. Welke verschillen tussen deze benaderingen?
Hoofdlijnen
- Goede hond of slechte hond? Nieuw onderzoek toont aan dat ras niet echt een voorspeller van gedrag is
- Welk vermelde molecuul zal het meest waarschijnlijk osmose in het lichaam veroorzaken?
- Waarom was de evolutie van nucleïnezuren belangrijk voor protocellen?
- Waar wordt abscisinezuur geproduceerd in een plant?
- Etiketten op verpakt vlees die de versheid weergeven, kunnen de houdbaarheidsdata vervangen, waardoor voedselverspilling wordt verminderd
- Wat doet de verkeerde pH om een enzym vorm te geven?
- Waarom bevindt DNA zich op de kern?
- Welk woord beschrijft de naamgeving van organismen?
- Waar wordt genetische informatie gedragen in DNA?
- Onderzoekers vinden dat intermoleculaire krachten clusters stabiliseren, aërosolproductie bevorderen

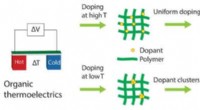
- Hoe restwarmte-energie op te vangen met verbeterde polymeren
- Goedkoop, energiezuinige en schone reactie om chemische grondstof te maken
- Krachtigste en mildste reagentia verkregen op basis van milieuvriendelijk jodium

- Wetenschappers ontwikkelen computergestuurde strategie om materiaalontdekking te versnellen

 Gevild karkas van zeeotter gevonden op strand in Californië
Gevild karkas van zeeotter gevonden op strand in Californië Wanneer platen langs elkaar glijden bij een transformatiegrens Welk geologisch proces zal het meest waarschijnlijk optreden?
Wanneer platen langs elkaar glijden bij een transformatiegrens Welk geologisch proces zal het meest waarschijnlijk optreden?  Wat hoeven elektromagnetische golven geen energie over te dragen?
Wat hoeven elektromagnetische golven geen energie over te dragen?  Studie biedt aanwijzingen over hoe klimaat de pandemie van 1918 beïnvloedde
Studie biedt aanwijzingen over hoe klimaat de pandemie van 1918 beïnvloedde Een stap opzij, interne getijden:supercomputermodellering verbetert de nauwkeurigheid van de hoogtemeting van satellieten
Een stap opzij, interne getijden:supercomputermodellering verbetert de nauwkeurigheid van de hoogtemeting van satellieten  Wanneer is snelheid belangrijk?
Wanneer is snelheid belangrijk?  Los Angeles County stemt om olie- en gasboringen uit te faseren
Los Angeles County stemt om olie- en gasboringen uit te faseren Nieuwe inzichten in gebroken symmetrieën:toepassing van de reciproke stelling van Lorentz op vloeistoffen met oneven viscositeiten
Nieuwe inzichten in gebroken symmetrieën:toepassing van de reciproke stelling van Lorentz op vloeistoffen met oneven viscositeiten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

