
Wetenschap
Niet-polaire covalente bindingen begrijpen:gelijke elektronendeling
Dit is waarom:
* Polariteit: De term "polair" verwijst naar de verdeling van elektrische lading binnen een molecuul. Bij een niet-polaire covalente binding worden de elektronen gelijkelijk verdeeld, wat betekent dat er geen significant verschil in lading is tussen de twee atomen.
* Elektronegativiteit: Elektronegativiteit is een maatstaf voor het vermogen van een atoom om elektronen aan te trekken. Wanneer twee atomen vergelijkbare elektronegativiteitswaarden hebben, delen ze elektronen gelijkelijk, wat resulteert in een niet-polaire covalente binding.
Voorbeelden van niet-polaire covalente bindingen:
* H₂ (waterstofgas): Beide waterstofatomen hebben dezelfde elektronegativiteit, dus delen ze de elektronen gelijk.
* O₂ (zuurstofgas): Beide zuurstofatomen hebben dezelfde elektronegativiteit, dus delen ze de elektronen gelijk.
* Cl₂ (chloorgas): Beide chlooratomen hebben dezelfde elektronegativiteit, dus delen ze de elektronen gelijk.
Belangrijkste afhaalpunten: Bij niet-polaire covalente bindingen worden de elektronen gelijkelijk verdeeld over de atomen, wat resulteert in een evenwichtige verdeling van de lading.
 Wat kunnen dichtheidsmassa en volume helpen om u te vertellen over een stof?
Wat kunnen dichtheidsmassa en volume helpen om u te vertellen over een stof?  Wat is het oxidatienummer van N in (N2H5) 2SO4?
Wat is het oxidatienummer van N in (N2H5) 2SO4?  Wat is een product van het elektrolyserwater dat KNO3 met een lage concentratie bevat?
Wat is een product van het elektrolyserwater dat KNO3 met een lage concentratie bevat?  De chemische formule voor een ionische verbinding vertegenwoordigt de?
De chemische formule voor een ionische verbinding vertegenwoordigt de?  Van superafdichtingen tot de detectie van gevaarlijke kabels dankzij ionenstralen
Van superafdichtingen tot de detectie van gevaarlijke kabels dankzij ionenstralen
 Onderzoeker:Klimaatmodellen kunnen maandenlang op supercomputers draaien, maar mijn nieuwe algoritme kan ze tien keer sneller maken
Onderzoeker:Klimaatmodellen kunnen maandenlang op supercomputers draaien, maar mijn nieuwe algoritme kan ze tien keer sneller maken  Nieuwe plaatsing voor een van de grootste massa-extincties op aarde
Nieuwe plaatsing voor een van de grootste massa-extincties op aarde Het kleinste element ter wereld?
Het kleinste element ter wereld?  NASA's nieuwe chef verandert van gedachten, gelooft nu in klimaatverandering
NASA's nieuwe chef verandert van gedachten, gelooft nu in klimaatverandering Uit een Canadees onderzoek blijkt dat eten zoals wij dat doen schadelijk is voor ons en de planeet
Uit een Canadees onderzoek blijkt dat eten zoals wij dat doen schadelijk is voor ons en de planeet
Hoofdlijnen
- Wat is de site van DNA -replicatie in eukaryoten?
- Wat laat mitose organismen toe?
- Hoe draagt DNA bij aan mitose?
- Bevatten alle levende wezens DNA?
- Welk type weefsel kan contracteren?
- Wat is urushiol?
- Wat gebeurt er met DNA vóór celdeling bij mitose?
- Hoe een 290 miljoen jaar oude boom de atoombom van Hiroshima overleefde
- Naamloze soorten bacteriën een naam geven in het tijdperk van big data
- Hoe het aantal neutronen te bepalen met behulp van het periodiek systeem

- Snelle screeningmachine kan eiwitsequenties lezen en scheiden
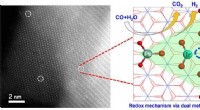
- Wetenschappers stellen redoxmechanisme voor water-gasverschuivingsreactie voor
- Een nieuwe techniek om goedkoper en efficiënter chloor te produceren

- Onderzoekers identificeren breekpunt van geleidend materiaal

 Die cafeïne in je drankje:is dat echt 'natuurlijk'?
Die cafeïne in je drankje:is dat echt 'natuurlijk'?  Wat is een lange buis die de magma -kamer verbindt met de oppervlakte?
Wat is een lange buis die de magma -kamer verbindt met de oppervlakte?  Waarom is de kracht van Upthrust hoger in heet water dan koud water?
Waarom is de kracht van Upthrust hoger in heet water dan koud water?  Is zure regen schadelijk voor dieren?
Is zure regen schadelijk voor dieren?  Wat zijn de 5 regels als u elektriciteit gebruikt?
Wat zijn de 5 regels als u elektriciteit gebruikt?  Om de vervuiling te verminderen, beleidsmakers moeten de focus verruimen tot verder dan schoorstenen
Om de vervuiling te verminderen, beleidsmakers moeten de focus verruimen tot verder dan schoorstenen Studie ontdekt hoe sommige eencellige organismen microbiomen controleren
Studie ontdekt hoe sommige eencellige organismen microbiomen controleren  Paddenstoelbegrafeniskostuum creëert leven na de dood
Paddenstoelbegrafeniskostuum creëert leven na de dood
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

