
Wetenschap
Elektronaffiniteit:definitie, proces en energieverandering
Hier is een overzicht:
* Neutraal gasvormig atoom: We beginnen met een atoom in zijn gasvormige toestand, niet gebonden aan andere atomen.
* Elektronentoevoeging: Er wordt een elektron toegevoegd aan de elektronenwolk van het atoom.
* Negatief ion: De toevoeging van het elektron resulteert in de vorming van een negatief geladen ion.
* Energieverandering: Bij dit proces kan energie vrijkomen (exotherm, negatieve elektronenaffiniteit) of energie-invoer vereisen (endotherm, positieve elektronenaffiniteit).
In eenvoudiger bewoordingen: Elektronenaffiniteit meet hoeveel een atoom een elektron "wil" verwerven.
Hier is een voorbeeld:
Chloor (Cl) heeft een hoge elektronenaffiniteit. Wanneer een chlooratoom een elektron verkrijgt om een chloride-ion (Cl-) te vormen, komt er energie vrij. Dit betekent dat chloor een sterke aantrekkingskracht heeft op elektronen.
Belangrijkste punten om te onthouden:
* Elektronenaffiniteit is een thermochemisch eigendom, wat betekent dat het zich bezighoudt met energieveranderingen.
* Elektronenaffiniteit wordt gewoonlijk uitgedrukt in elektronvolt (eV) of kilojoule per mol (kJ/mol) .
* Het is belangrijk op te merken dat de elektronenaffiniteit een periodieke trend is , doorgaans stijgend over een bepaalde periode en afnemend per groep.
Hoofdlijnen
- Wat hebben dierencellen die plant hebben?
- Laat je huisdier niet per ongeluk dronken worden dit gekke seizoen (sorry Tiddles)
- Waarom leven dieren in de Dode Zee?
- Wat zijn twee producten van biotechnologie?
- Begrijpen waarom BRCA2 verband houdt met het risico op kanker
- Wat gebeurt er als een persoon min of meer chromosomen heeft?
- Vleesetende planten inspireren slimme gladde oppervlakken en bionische robots
- Hoe kunnen enzymnamen worden herkend?
- Wat beschrijft een verschil tussen transcriptie en DNA -replicatie?
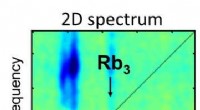
- Onderzoekers passen voor het eerst 2D-spectroscopie toe op geïsoleerde moleculaire systemen
- Even kijken hoe ijsvorming voorruiten kan houden, hoogspanningsleidingen ijsvrij

- Nieuw composietmateriaal dat zichzelf kan afkoelen onder extreme temperaturen

- Nieuwe sonde met superresolutie legt cellen in ongekend detail vast
- Video:Hoe lood (misschien) de ondergang van het oude Rome veroorzaakte

 Zonder wrijving zouden alle lichamen in hetzelfde tempo vallen?
Zonder wrijving zouden alle lichamen in hetzelfde tempo vallen?  Welke fase wordt volledig overgeslagen tijdens sublimatie en afzetting?
Welke fase wordt volledig overgeslagen tijdens sublimatie en afzetting?  Hoe hebben geologen vastgesteld dat de westkust van Californië een hoger aardbevingsrisico heeft dan andere gebieden in de VS?
Hoe hebben geologen vastgesteld dat de westkust van Californië een hoger aardbevingsrisico heeft dan andere gebieden in de VS?  Wat doet een structuur?
Wat doet een structuur?  Wat is de temperatuur welk magnetisch materiaal een permanente magnetisatie kan behouden?
Wat is de temperatuur welk magnetisch materiaal een permanente magnetisatie kan behouden?  Grafenen die licht laten schijnen, kunnen leiden tot supersnel internet
Grafenen die licht laten schijnen, kunnen leiden tot supersnel internet Wat definieert een sappige plant of blad?
Wat definieert een sappige plant of blad?  Wat is het kookpunt van ninhydrin?
Wat is het kookpunt van ninhydrin?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


