
Wetenschap
pH van water bij 70°C:berekening en begrip
Inzicht in de pH en temperatuur
* pH: Een maatstaf voor de zuurgraad of alkaliteit van een oplossing. Het is gebaseerd op de concentratie waterstofionen (H+).
* Temperatuur: Naarmate de temperatuur stijgt, neemt de dissociatie van watermoleculen (H2O → H+ + OH-) toe. Dit betekent dat er meer waterstofionen (H+) aanwezig zijn, wat leidt tot een lagere pH (zuurder).
Berekening
1. Ionenproduct van water (Kw): Bij 25°C is Kw 1,0 x 10^-14. Kw verandert echter met de temperatuur.
2. Kw bij 70°C: Om de Kw-waarde bij 70°C te vinden, heb je een tabel of vergelijking nodig. De waarde is ongeveer 2,5 x 10^-13.
3. Bereken de H+-concentratie:
* Kw =[H+][OH-]
* Omdat zuiver water gelijke concentraties H+ en OH- heeft, kunnen we dit vereenvoudigen tot:Kw =[H+]^2
* [H+] =√Kw =√(2,5 x 10^-13) ≈ 5,0 x 10^-7 M
4. pH-berekening:
* pH =-log[H+]
* pH =-log(5,0 x 10^-7) ≈ 6,3
Resultaat: De pH van zuiver water bij 70°C is ongeveer 6,3 .
Belangrijke opmerking: Hoewel de pH iets lager is dan 7, wordt zuiver water van 70°C nog steeds als neutraal beschouwd omdat de concentraties H+ en OH- gelijk zijn.
 Kleine huizen zien er prachtig uit, maar hebben een donkere kant:drie dingen die ze je niet vertellen over marketing-blurb
Kleine huizen zien er prachtig uit, maar hebben een donkere kant:drie dingen die ze je niet vertellen over marketing-blurb Koelende rol van fijnstof bij opwarming aarde sterker dan eerder gedacht
Koelende rol van fijnstof bij opwarming aarde sterker dan eerder gedacht Hugo, ik en iedereen:Doe mee aan de oorlog tegen plasticvervuiling
Hugo, ik en iedereen:Doe mee aan de oorlog tegen plasticvervuiling Feiten over zijderupsen
Feiten over zijderupsen  Veranderingen in de Antarctische mariene ecosystemen
Veranderingen in de Antarctische mariene ecosystemen
Hoofdlijnen
- Welke organellen zijn er in de Elodea -bladcellen die het anders maken dan een dierencel?
- Hoe reproduceren dierenachtige protisten zich voort?
- Wat is cyberchondrie?
- Waar bestaat een bloemcel uit?
- Hoe zijn gegevens waardevol voor wetenschappers?
- Welke botten zijn staaf gevormd in het lichaam?
- Hoe reageren bacteriën op hun omgeving?
- Wat betekent de uitdrukking oor tot grond?
- Wat zijn de 2 microscopische organismen die ziekten veroorzaken?
- Verbeterd begrip van industriële elektrodeprocessen

- Extreem sterke en toch ongelooflijk ductiele meercomponentenlegeringen ontwikkeld

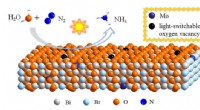
- Verbeterde fotosynthese van ammoniak in de omgeving met behulp van nanosheets met lichtschakelbare zuurstofvacatures
- Gesprek tussen een bioloog en een filosoof:is de mens een halfgod geworden?

- Onderzoekers klokken DNA's hersteltijd na chemotherapie

 Ceria-zirconia-nanodeeltjes als verbeterde multi-antioxidanten zijn effectief bij de behandeling van sepsis
Ceria-zirconia-nanodeeltjes als verbeterde multi-antioxidanten zijn effectief bij de behandeling van sepsis Hoe heeft de zon een uitgezonden energie?
Hoe heeft de zon een uitgezonden energie?  Wat is het eigendom van mineralen die breken met grillige oppervlakken?
Wat is het eigendom van mineralen die breken met grillige oppervlakken?  Wat is het ionische karakter van bariumoxide?
Wat is het ionische karakter van bariumoxide?  Opruimen met cellulose
Opruimen met cellulose Kleine batterij is ook een nanomotor
Kleine batterij is ook een nanomotor Hoe is de studie van de aarde en zijn mensen geroepen?
Hoe is de studie van de aarde en zijn mensen geroepen?  Wereldwijde luchthavencapaciteitscrisis te midden van passagiersboom:IATA
Wereldwijde luchthavencapaciteitscrisis te midden van passagiersboom:IATA
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

