
Wetenschap
Voorspellen van producten van metaalzuurreacties:carbonaten en oxiden
De reacties begrijpen
* Metalen met zuren: Dit is een enkele verdringingsreactie waarbij een metaal (doorgaans reactiever dan waterstof) waterstof uit een zuur verdringt.
* Metaalcarbonaten met zuren: Het zuur reageert met het carbonaat en produceert kooldioxidegas, water en een zout.
* Metaaloxiden met zuren: Het zuur reageert met het oxide en produceert water en een zout.
De producten voorspellen
1. Identificeer de reactanten:
* Metaal: Het metaal zal het elementsymbool zijn (bijvoorbeeld Mg, Zn, Fe).
* Zuur: Veel voorkomende zuren zijn zoutzuur (HCl), zwavelzuur (H₂SO₄) en salpeterzuur (HNO₃).
* Metaalcarbonaat: Het carbonaat heeft de formule M₂CO₃ (waarbij M het metaal voorstelt).
* Metaaloxide: Het oxide heeft de formule MO (waarbij M het metaal voorstelt).
2. Identificeer de producten:
* Metalen + Zuren:
* Zout: Het zout zal worden gevormd uit het metaalkation en het zuuranion. Bijvoorbeeld:
* Mg + HCl → MgCl₂ + H₂ (Magnesiumchloride)
* Zn + H₂SO₄ → ZnSO₄ + H₂ (Zinksulfaat)
* Metaalcarbonaten + zuren:
* Zout: Het zout zal worden gevormd uit het metaalkation en het zuuranion.
* Kooldioxide: CO₂ (gas)
* Water: H₂O
* CaCO₃ + 2HCl → CaCl₂ + CO₂ + H₂O (Calciumchloride)
* Na₂CO₃ + H₂SO₄ → Na₂SO₄ + CO₂ + H₂O (natriumsulfaat)
* Metaaloxiden + zuren:
* Zout: Het zout zal worden gevormd uit het metaalkation en het zuuranion.
* Water: H₂O
* CuO + 2HNO₃ → Cu(NO₃)₂ + H₂O (Koper(II)nitraat)
* Fe₂O₃ + 3H₂SO₄ → Fe₂(SO₄)₃ + 3H₂O (ijzer(III)sulfaat)
De chemische vergelijkingen in evenwicht brengen
Nadat je de producten hebt geïdentificeerd, zorg je ervoor dat de chemische vergelijking in evenwicht is door de coëfficiënten (de getallen vóór elke chemische formule) aan te passen, zodat het aantal atomen van elk element aan beide kanten van de vergelijking hetzelfde is.
Belangrijke overwegingen
* Reactiviteit: Niet alle metalen reageren met alle zuren. De reactiviteit van het metaal en de sterkte van het zuur spelen een rol. U kunt een reactiviteitsreeks van metalen raadplegen om te voorspellen of er een reactie zal optreden.
* Oplosbaarheid: De gevormde zouten kunnen oplosbaar of onoplosbaar zijn in water.
Voorbeeld:
Laten we de producten van de reactie tussen zinkmetaal en zwavelzuur voorspellen:
1. Reactanten: Zn (zink), H₂SO₄ (zwavelzuur)
2. Producten: ZnSO₄ (zinksulfaat), H₂ (waterstofgas)
3. Gebalanceerde vergelijking: Zn + H₂SO₄ → ZnSO₄ + H₂
Laat het me weten als je meer voorbeelden wilt doornemen!
 Wat is de term die wordt gebruikt om alle lucht rond de aarde te beschrijven?
Wat is de term die wordt gebruikt om alle lucht rond de aarde te beschrijven?  Plantendiversiteit slachtoffer van zeer ernstige bosbranden
Plantendiversiteit slachtoffer van zeer ernstige bosbranden Wat zijn de dominante planten in een tropisch regenwoud?
Wat zijn de dominante planten in een tropisch regenwoud?  Wat zijn verschil en overeenkomsten tussen het ecosysteem van gemeenschappen?
Wat zijn verschil en overeenkomsten tussen het ecosysteem van gemeenschappen?  Grote gegevens, machine learning werpt licht op Aziatische herbebossingssuccessen
Grote gegevens, machine learning werpt licht op Aziatische herbebossingssuccessen
Hoofdlijnen
- Wat is er waarschijnlijk waar over de evolutionaire geschiedenis van organisme en kippen?
- Studie geeft inzicht in hoe algen kooldioxide uit de lucht zuigen
- NOAA-rapporten laten sterke economische voordelen uit de visserij zien en een aanhoudende verbetering van de visbestanden
- Wat zijn de componenten van een plantencel?
- Hoe kan een enkel RNA -transcript worden vertaald in verschillende polypeptiden?
- Welke van de volgende paden produceert de meeste NADH en de minste ATP?
- Hoe is het bloedsomloop van glucose betrokken?
- Wat zijn de verschillende segmenten van DNA die codeer zijn voor specifieke eiwitten die worden genoemd?
- Waarom zie je de kern in ELODEA plantencel?
- Onderzoekers ontdekken een manier om de kleur van OLED's te controleren
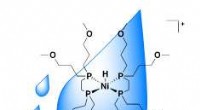
- Nieuwe nikkelkatalysator werkt in water om broeikasgas om te zetten in chemische grondstof
- Nieuwe biochemische verbinding kan milieuverontreinigende stoffen afbreken

- Koelere katalysatoren:schonere lucht voor iedereen

- Scherp smakende substantie in gember vermindert slechte adem

 Hoe bereidt u de PPM -oplossing van Solid voor?
Hoe bereidt u de PPM -oplossing van Solid voor?  Hoe vermindert een muur de overdracht van thermische energie?
Hoe vermindert een muur de overdracht van thermische energie?  NASA's OSIRIS-APEX ongedeerd na een verschroeiende zon
NASA's OSIRIS-APEX ongedeerd na een verschroeiende zon  Zoetwaterstralen en ecosysteemcomponenten
Zoetwaterstralen en ecosysteemcomponenten  Welke planten zijn betrokken bij fotosynthese?
Welke planten zijn betrokken bij fotosynthese?  Welke verbinding bestaat uit vier elementen?
Welke verbinding bestaat uit vier elementen?  Galileos-experiment met vrij vallende objecten slaagt voor ruimtetest en bewijst het equivalentieprincipe verder
Galileos-experiment met vrij vallende objecten slaagt voor ruimtetest en bewijst het equivalentieprincipe verder Ondernemers willen spookvissen beëindigen
Ondernemers willen spookvissen beëindigen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

