
Wetenschap
Covalente versus metaalobligaties:belangrijkste verschillen verklaard
Covalente obligaties
* Formatie: Gevormd wanneer twee niet-metaalatomen elektronen delen om een stabiele elektronenconfiguratie te bereiken (gevulde buitenschil).
* Elektronen delen: Elektronen worden gelijkelijk (niet-polair) of ongelijkmatig (polair) verdeeld tussen atomen.
* Verbindingssterkte: Kan sterk of zwak zijn, afhankelijk van het type covalente binding.
* Eigenschappen:
* Vormen doorgaans moleculen met lage smelt- en kookpunten.
* Slechte geleiders van elektriciteit (behalve grafiet).
* Kan bij kamertemperatuur vaste stoffen, vloeistoffen of gassen zijn.
* Hebben vaak een lage treksterkte.
* Voorbeelden: Water (H₂O), kooldioxide (CO₂), methaan (CH₄)
Metaalverbindingen
* Formatie: Gevormd tussen metaalatomen waar elektronen worden gedelokaliseerd (vrij om door de hele structuur te bewegen).
* Elektronen delen: Elektronen zijn niet gelokaliseerd tussen specifieke atomen, maar vormen een "zee" van elektronen die worden gedeeld door alle atomen in de metaalstructuur.
* Verbindingssterkte: Over het algemeen sterk vanwege de aantrekkingskracht tussen de positieve metaalionen en de zee van gedelokaliseerde elektronen.
* Eigenschappen:
* Uitstekende geleiders van warmte en elektriciteit.
* Buigzaam (kan tot platen worden gehamerd).
* Nodulair (kan tot draden worden getrokken).
* Hebben doorgaans hoge smelt- en kookpunten.
* Voorbeelden: IJzer (Fe), koper (Cu), goud (Au)
Hier is een tabel met een samenvatting van de belangrijkste verschillen:
| Kenmerk | Covalente binding | Metaalbinding |
|------------------|--------------|-------------|
| Betrokken atomen | Niet-metalen | Metalen |
| Elektronen delen | Gedeeld tussen specifieke atomen | Gedelokaliseerd, gedeeld door alle atomen |
| Hechtsterkte | Variabel | Sterk |
| Geleidbaarheid | Slecht | Uitstekend |
| Maakbaarheid | Niet kneedbaar | Kneedbaar |
| Ductiliteit | Niet ductiel | Nodulair |
| Smelten/koken Pt | Laag | Hoog |
In essentie:
* Covalente bindingen omvatten het delen van elektronen tussen specifieke atomen, resulterend in moleculen.
* Metaalverbindingen waarbij sprake is van een ‘zee’ van gedelokaliseerde elektronen die door alle atomen in de structuur worden gedeeld, wat leidt tot de unieke eigenschappen van metalen.
 Science Experiment Ideas: Epsom Salts
Science Experiment Ideas: Epsom Salts  Welk type binding zal zich vormen tussen broom en broom?
Welk type binding zal zich vormen tussen broom en broom?  Zijn binaire moleculaire verbindingen gemaakt van twee kationen?
Zijn binaire moleculaire verbindingen gemaakt van twee kationen?  Chloorgebruik:waterdesinfectie en bleekmiddelproductie - [uw merk/sitenaam]
Chloorgebruik:waterdesinfectie en bleekmiddelproductie - [uw merk/sitenaam]  Wanneer ijzer corrodeert in aanwezigheid van lucht en water om wat te vormen?
Wanneer ijzer corrodeert in aanwezigheid van lucht en water om wat te vormen?
Hoofdlijnen
- Welk gebied leven en werken organismen?
- RNA-ontdekking kan de plantwarmte helpen verhogen, droogtetolerantie
- Vergelijk de van organismen die zich benemen met die fotosynthetize?
- De takken van de wetenschap staan niet van elkaar gescheiden. Waar of niet waar?
- Is maretak meer dan alleen een excuus voor een kus?
- Waar wordt het celmembraan gevonden?
- Wat is het weefsel van het skeletsysteem?
- Wat is de functie van begeleidende cellen?
- Hoe reproduceert een Yersinia -pestis zich?
- Micro-organismen bouwen de beste brandstofefficiënte waterstofcellen
- Maak een realistisch aluminiumatoommodel voor klassikaal leren

- Ongebruikelijk halfmetaal vertoont bewijs van unieke toestanden van oppervlaktegeleiding

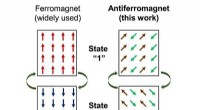
- Antiferromagnetische materialen grote stap richting commerciële toepassing
- Onderzoekers rapporteren bio-geïnspireerde selectieve antibiotica
 Van welk principe is de calorimetrie afhankelijk?
Van welk principe is de calorimetrie afhankelijk?  Wat is de celorganel die betrokken is bij het proces van fotosynthese?
Wat is de celorganel die betrokken is bij het proces van fotosynthese?  Samenwerking leidt tot succes:menselijk onderzoek en bacteriële quorumdetectie
Samenwerking leidt tot succes:menselijk onderzoek en bacteriële quorumdetectie  Hoe verschillen virussen van levende organismen?
Hoe verschillen virussen van levende organismen?  Hoe werden de Carlsbad -grotten gevormd?
Hoe werden de Carlsbad -grotten gevormd?  Onderzoek vindt dat gezondheid niet het enige probleem is met bacteriegroei
Onderzoek vindt dat gezondheid niet het enige probleem is met bacteriegroei Diamanten zijn de beste vriend van een sonde
Diamanten zijn de beste vriend van een sonde Er zijn sommige cellen die niet door mitose kunnen gaan, met andere woorden, een organisme maakt nieuwe wanneer de sterf en spiervoorbeelden van de matrijzen?
Er zijn sommige cellen die niet door mitose kunnen gaan, met andere woorden, een organisme maakt nieuwe wanneer de sterf en spiervoorbeelden van de matrijzen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

