
Wetenschap
Ionische geleidbaarheid in oplossingen:een uitgebreide uitleg
* Ionische verbindingen: Deze verbindingen worden gevormd door de elektrostatische aantrekking tussen positief geladen ionen (kationen) en negatief geladen ionen (anionen).
* Oplossen in water: Wanneer een ionische verbinding in water oplost, omringen de watermoleculen de ionen en trekken ze uit elkaar, waardoor de ionische bindingen worden verbroken. Dit proces wordt dissociatie genoemd.
* Gratis ionen: De opgeloste ionen kunnen nu zelfstandig in de oplossing bewegen.
* Elektrische geleidbaarheid: Deze vrij bewegende ionen fungeren als ladingsdragers. Wanneer een potentiaalverschil (spanning) over de oplossing wordt aangelegd, bewegen de positieve ionen naar de negatieve elektrode (kathode) en de negatieve ionen naar de positieve elektrode (anode). Deze ladingsstroom vormt een elektrische stroom, waardoor de oplossing geleidend wordt.
Voorbeeld: Natriumchloride (NaCl) is een ionische verbinding. Wanneer opgelost in water, dissocieert het in Na+ en Cl-ionen. Deze vrije ionen zorgen ervoor dat de oplossing elektriciteit kan geleiden.
Belangrijke opmerking: Ionische verbindingen geleiden *geen* elektriciteit in hun vaste toestand, omdat de ionen vastzitten in een stijve roosterstructuur en niet vrij kunnen bewegen.
 Metaalbinding versus covalente binding:waarom metalen geen gigantische covalente structuren vormen
Metaalbinding versus covalente binding:waarom metalen geen gigantische covalente structuren vormen  Hoe kunnen onoplosbare deeltjes uit een hete oplossing worden verwijderd?
Hoe kunnen onoplosbare deeltjes uit een hete oplossing worden verwijderd?  Wat is een groter fluoratoom of chlooratoom?
Wat is een groter fluoratoom of chlooratoom?  Wat is de massa voor aluminium chloraatformule?
Wat is de massa voor aluminium chloraatformule?  Zure regenverontreinigende stoffen:zwaveldioxide en stikstofoxiden uitgelegd
Zure regenverontreinigende stoffen:zwaveldioxide en stikstofoxiden uitgelegd
 Hoe een biovriendelijke meststof een groenere manier kan bieden om planten te laten groeien
Hoe een biovriendelijke meststof een groenere manier kan bieden om planten te laten groeien De relatie tussen abiotische en biotische componenten van een ecosysteem in het bos
De relatie tussen abiotische en biotische componenten van een ecosysteem in het bos Verwaterde biodiversiteit:het type monster is van cruciaal belang in milieu-DNA-onderzoeken voor biomonitoring
Verwaterde biodiversiteit:het type monster is van cruciaal belang in milieu-DNA-onderzoeken voor biomonitoring Wat is uniek aan het water op aarde?
Wat is uniek aan het water op aarde?  Nieuwe bronnen ondersteunen stammen bij de voorbereiding op klimaatverandering
Nieuwe bronnen ondersteunen stammen bij de voorbereiding op klimaatverandering
Hoofdlijnen
- Wat is Eurobacteria?
- Bacteriële ademhaling uitgelegd:aërobe versus anaërobe processen
- Hoe zeer resistente schimmelstammen ontstaan
- Wat beschrijft speciatie?
- RNA-productie:transcriptie en RNA-polymerase begrijpen
- Wat is het verschil tussen een prokaryote -cel en eukaryote -cel?
- Wanneer citroenen je leven geven:Herpetofauna-aanpassing aan citrusboomgaarden in Belize
- Denk je dat krekels raar zijn? Kijk eens naar superfans, die de insecten opeten, gebruiken in de kunst en zelfs striptease
- Wat is een voordeel van prezygotisch isolement en postzygotisch isolement?
- Een nieuwe manier om methaan direct om te zetten in methanol met behulp van goud-palladium nanodeeltjes

- Een nieuwe generatie kunstmatige netvliezen op basis van 2D-materialen

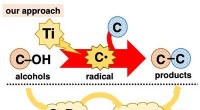
- Alcoholen als voorlopers van koolstofradicaal
- Kleine magnetische deeltjes zorgen ervoor dat nieuw materiaal kan buigen, twist, en grijp

- Neutronenstudie van glaucoommedicijnen biedt aanwijzingen over enzymdoelen voor agressieve kankers

 Hoe het gebruik van natuurlijke hulpbronnen te verminderen
Hoe het gebruik van natuurlijke hulpbronnen te verminderen Wat is thermische efficiëntie?
Wat is thermische efficiëntie?  Hoe een nieuwe klasse sulfonamiden de overdracht van malaria krachtig blokkeert
Hoe een nieuwe klasse sulfonamiden de overdracht van malaria krachtig blokkeert  Wat is taxonomie in Drupal?
Wat is taxonomie in Drupal?  Waarom is de kracht uit balans als er een appel aan een boom hangt?
Waarom is de kracht uit balans als er een appel aan een boom hangt?  De houtkap van tientallen jaren vormt nog steeds een bedreiging voor gevlekte uilen in nationale bossen
De houtkap van tientallen jaren vormt nog steeds een bedreiging voor gevlekte uilen in nationale bossen Waarom het afgelegen Antarctica zo belangrijk is in een opwarmende wereld
Waarom het afgelegen Antarctica zo belangrijk is in een opwarmende wereld Gigantische verbetering van elektromagnetische golven onthuld in kleine diëlektrische deeltjes
Gigantische verbetering van elektromagnetische golven onthuld in kleine diëlektrische deeltjes
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

