
Wetenschap
Waterstofionen begrijpen:de kern van zuren
Dit is waarom:
* Arrhenius-definitie: Deze klassieke definitie stelt dat een zuur een stof is die waterstofionen (H+) produceert wanneer deze in water wordt opgelost.
* Brønsted-Lowry-definitie: Deze bredere definitie zegt dat een zuur een stof is die een proton (H+) doneert.
Voorbeelden:
* Zoutzuur (HCl): Wanneer opgelost in water, dissocieert HCl in H+ en Cl-ionen.
* Zwavelzuur (H2SO4): Dit sterke zuur doneert twee protonen, waardoor 2H+ en SO4^2- ionen worden gevormd.
Belangrijke opmerking: Hoewel zuren altijd H+-ionen hebben, kunnen ze ook andere ionen bevatten, afhankelijk van het specifieke zuur. Zwavelzuur (H2SO4) heeft bijvoorbeeld naast waterstofionen ook sulfaationen (SO4^2-).
 Ionische lading van loodcarbonaat:neutraliteit begrijpen
Ionische lading van loodcarbonaat:neutraliteit begrijpen  Hoeveel moleculen zitten er in één mol zwaveldioxide SO2?
Hoeveel moleculen zitten er in één mol zwaveldioxide SO2?  Wat is de chemische formule voor Greiss -reagens?
Wat is de chemische formule voor Greiss -reagens?  Wat is de vorm van de grafiek bij smelt- en vriespunten van water. Wat vertelt dit je over de temperatuur?
Wat is de vorm van de grafiek bij smelt- en vriespunten van water. Wat vertelt dit je over de temperatuur?  Wat zou er gebeuren als materialen niet vervallen?
Wat zou er gebeuren als materialen niet vervallen?
 Studie belicht complexe oorzaken van overstromingen op de Malediven
Studie belicht complexe oorzaken van overstromingen op de Malediven VS ontdooit uit Arctische diepvries terwijl dodental stijgt
VS ontdooit uit Arctische diepvries terwijl dodental stijgt Amerikaans onderzoek toont aan dat pesticiden de bedreigde zalm schaden, walvissen
Amerikaans onderzoek toont aan dat pesticiden de bedreigde zalm schaden, walvissen Hoe maak je een Diorama van een Spider Habitat
Hoe maak je een Diorama van een Spider Habitat  Nieuwe studie herdefinieert begrip van waar ijsbergen smeltwater in de Zuidelijke Oceaan brengen
Nieuwe studie herdefinieert begrip van waar ijsbergen smeltwater in de Zuidelijke Oceaan brengen
Hoofdlijnen
- Hoe minder eten in het vroege leven zou kunnen helpen bij de voortplanting later
- Wordt overdracht RNA gevonden in cytosol?
- Wanneer de allelen aanwezig zijn voor een eigenschap hetzelfde zijn. genen genaamd?
- Moet het 'extreme fokken' van teckels en Franse buldoggen verboden worden?
- Wat is de subeenheidstructuur van nucleïnezuur?
- Hoe microscopen een revolutie teweegbrachten in de moderne wetenschap
- Waar staat mevrouw Nerg voor in de wetenschap zoals bewegingsreproductie .......?
- Wat is Polykaryon?
- Waarom maken bijen minder honing? Studie onthult aanwijzingen uit vijf decennia aan gegevens
- Chemische energie begrijpen:van biologische processen tot motorverbranding

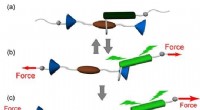
- Nieuwsgierige in elkaar grijpende moleculen vertonen een dubbele respons
- Belangrijkste bouwsteen voor organische moleculen ontdekt in meteorieten

- Een zachtere, nauwkeurigere lasersnijtechniek

- Raamwerkdiversiteit van koolstofnitrides biedt een rijk platform voor katalyse met één atoom

 Wat voor soort telescoop gebruikte Caroline Herschel in de ruimte?
Wat voor soort telescoop gebruikte Caroline Herschel in de ruimte?  Welk deel van een ster strekt zich miljoenen kilometer uit in de ruimte?
Welk deel van een ster strekt zich miljoenen kilometer uit in de ruimte?  Nieuwe inzichten in van der Waals materialen gevonden
Nieuwe inzichten in van der Waals materialen gevonden Hoe komt bacteriën over?
Hoe komt bacteriën over?  Hoe DNA-forensisch onderzoek verloren Nigeriaanse meisjes kan identificeren (update)
Hoe DNA-forensisch onderzoek verloren Nigeriaanse meisjes kan identificeren (update)  Diversificatie van vruchtwisseling verbetert de milieuresultaten en houdt boerderijen winstgevend
Diversificatie van vruchtwisseling verbetert de milieuresultaten en houdt boerderijen winstgevend Heeft de natuur een hand gehad bij de vorming van de Grote Sfinx?
Heeft de natuur een hand gehad bij de vorming van de Grote Sfinx?  Archeologische ontdekking levert aanwijzingen op over hoe onze voorouders hun omgeving mogelijk hebben aangepast
Archeologische ontdekking levert aanwijzingen op over hoe onze voorouders hun omgeving mogelijk hebben aangepast
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

