
Wetenschap
Chemische energie begrijpen:van biologische processen tot motorverbranding
Door Joseph Nicholson
Bijgewerkt op 30 augustus 2022
Wat is chemische energie?
Chemische energie wordt opgeslagen in de bindingen tussen atomen en moleculen. Wanneer een chemische reactie elektronen en protonen herschikt, komt er energie vrij of wordt deze geabsorbeerd. De wet van behoud van energie garandeert dat energie nooit wordt vernietigd, maar alleen wordt getransformeerd. Bij een reactie die de interne energie van het systeem verlaagt, wordt het teveel aan warmte of licht aan de omgeving afgegeven, terwijl een endotherme reactie energie aan de omgeving onttrekt.
Organische chemische reacties
Levende organismen zijn afhankelijk van chemische energie. Bij fotosynthese vangt chlorofyl zonlicht op om water in waterstof en zuurstof te splitsen. De vrijgekomen waterstof combineert met koolstofdioxide uit de atmosfeer om koolhydraten (glucose en andere suikers) op te bouwen die planten gebruiken voor de groei. Cellulaire ademhaling, het omgekeerde proces, oxideert deze koolhydraten met zuurstof om ATP te produceren, de universele energievaluta voor cellulaire functies.
Anorganische chemische reacties
Chemische energie beperkt zich niet tot de biologie. Verbranding in benzinemotoren is een chemische reactie waarbij koolwaterstofbrandstof reageert met zuurstof uit de lucht, waardoor de kracht wordt gegenereerd om een krukas te laten draaien. Vuurwerk, lucifers en glowsticks zijn ook afhankelijk van chemische bindingen:bij het verbranden van fosfor komt licht en warmte vrij, terwijl het geactiveerde chemische mengsel van een glowstick zichtbaar licht uitstraalt met minimale hitte.
Reactiesnelheden en kinetiek
De snelheid van een chemische reactie hangt af van verschillende controleerbare variabelen:concentratie van de reactanten, beschikbaar oppervlak, temperatuur en druk. Ingenieurs passen deze parameters aan om de productie te optimaliseren of ongewenste bijproducten in industriële processen te minimaliseren. Het begrijpen van de kinetiek is essentieel voor het veilig en efficiënt opschalen van reacties.
De rol van katalysatoren
Katalysatoren versnellen reacties zonder te worden verbruikt. In autokatalysatoren zetten metalen uit de platinagroep schadelijke uitlaatgassen (stikstofoxiden, koolmonoxide en onverbrande koolwaterstoffen) om in goedaardige stikstof, zuurstof, kooldioxide en water. Omdat de katalysator onveranderd blijft, kan deze talloze keren worden hergebruikt, waardoor het een hoeksteen is van de moderne emissiebeheersing.
Voor meer gedetailleerde uitleg, zie het Wikipedia-artikel over chemische energie .
 Chemische stoffen die stof vernietigen:een gids voor veelvoorkomende schade
Chemische stoffen die stof vernietigen:een gids voor veelvoorkomende schade  Hoe vind je een elektron in neutraal atoom?
Hoe vind je een elektron in neutraal atoom?  Wat lost in regenwater op om zure regen te maken?
Wat lost in regenwater op om zure regen te maken?  Wetenschappers vinden nieuw solid-state materiaal voor thermische regeling
Wetenschappers vinden nieuw solid-state materiaal voor thermische regeling Onderzoekers ontdekken wat sommige kippen waterefficiënter maakt dan andere
Onderzoekers ontdekken wat sommige kippen waterefficiënter maakt dan andere
Hoofdlijnen
- Hoe is de membraanpermeabiliteit?
- Beschrijf hoe microscopische zeeorganismen aardolie en aardgas vormen?
- Is een menselijk multicellulair organisme?
- Hoe heet een eenvoudig brein?
- Een mogelijke verklaring voor een reeks observaties of antwoord op de wetenschappelijke vraag is een?
- Wat zijn isolatiemedia in de microbiologie?
- Wat is de wetenschappelijke definitie voor probleemverklaring?
- Hoe je hersenen werken
- Hoe worden cellen georganiseerd in het meeste meercellig organisme?
- Onderzoekers maken röntgenfoto's van accu's van elektrische voertuigen terwijl ze na verloop van tijd verslechteren

- Oppervlaktebevochtigbaarheid heeft weinig effect op atmosferische waterverzameling, maar randstructuur is cruciaal

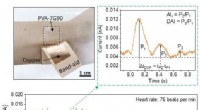
- Uitvinding biedt nieuwe optie voor het bewaken van de gezondheid van het hart
- Mechanisme van Cl-geïnitieerde oxidatie van methacroleïne onder NOx-vrije omstandigheden

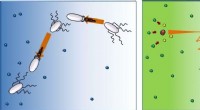
- Enzymen en bacteriën bewegen richting, maar bacteriën naar voedsel, enzymen weg
 Hoe heet een gat in de korst?
Hoe heet een gat in de korst?  Wat is het waterlichaam gedeeltelijk omsloten over land?
Wat is het waterlichaam gedeeltelijk omsloten over land?  Achter het gehuil van zonnewind, stille piepjes onthullen de oorsprong
Achter het gehuil van zonnewind, stille piepjes onthullen de oorsprong Hoe worden sterren gegroepeerd om een sterrenbeeld te maken?
Hoe worden sterren gegroepeerd om een sterrenbeeld te maken?  Chromosomale dynamiek van bevruchting:van meiose tot zygootvorming
Chromosomale dynamiek van bevruchting:van meiose tot zygootvorming  Wat is de smalle zone op Mid-Ocean Ridge Crest waar de meeste geologische activiteit plaatsvindt?
Wat is de smalle zone op Mid-Ocean Ridge Crest waar de meeste geologische activiteit plaatsvindt?  Wat is de chemische reactie in antacide -tabbladen?
Wat is de chemische reactie in antacide -tabbladen?  Verspreiden bacteriën en virus zich op dezelfde manier?
Verspreiden bacteriën en virus zich op dezelfde manier?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

