
Wetenschap
Waarom is boor een metalloïde in groep 13? - Periodiek systeem uitgelegd
Hier is de uitleg:
* Elektronische configuratie: Alle elementen in Groep 3A hebben 3 valentie-elektronen (elektronen in hun buitenste schil). Dit is het bepalende kenmerk van de groep. Boron heeft de elektronische configuratie van 2s²2p¹, net als de andere leden van de groep.
* Vergelijkbaar chemisch gedrag: Hoewel het chemische gedrag van Boron in sommige opzichten verschilt van de rest van de groep, vertoont het overeenkomsten in bepaalde reacties. Borium kan bijvoorbeeld verbindingen vormen met een oxidatietoestand van +3, vergelijkbaar met andere elementen in de groep.
Waarom is Boron echter anders?
Borium is een kleiner atoom vergeleken met de andere elementen in de groep. Dit resulteert in:
* Sterkere aantrekkingskracht tussen de kern en elektronen: Dit maakt Boron elektronegatiever en minder metaalachtig dan de rest van de groep.
* Hogere ionisatie-energie: Borium heeft meer energie nodig om een elektron te verwijderen, waardoor de niet-metallische aard ervan verder wordt ondersteund.
Dus hoewel Boron enkele metalloïde eigenschappen vertoont, wordt het in Groep 3A geplaatst vanwege zijn elektronische configuratie en vergelijkbaar chemisch gedrag in bepaalde aspecten. Door het kleinere formaat en de unieke eigenschappen van Boron onderscheidt het zich van de rest van de groep.
Het is belangrijk om te onthouden dat het periodiek systeem een voortdurend evoluerend systeem is, en dat de plaatsing van elementen soms een beetje een compromis kan zijn. De positie van Boron weerspiegelt de gedeelde elektronenconfiguratie en enkele chemische overeenkomsten met de andere groepsleden, ook al vertoont het verschillende eigenschappen.
 Wat komt er vrij wanneer de chemische binding verbroken tussen tweede en derde fosfaat van een ATP -molecuul?
Wat komt er vrij wanneer de chemische binding verbroken tussen tweede en derde fosfaat van een ATP -molecuul?  Wat betekent alkalische fosfatas?
Wat betekent alkalische fosfatas?  Wat is de formule voor metalen ijzer?
Wat is de formule voor metalen ijzer?  Magnesium + zoutzuurreactie:evenwichtige vergelijking en uitleg
Magnesium + zoutzuurreactie:evenwichtige vergelijking en uitleg  Nieuwe polymeermaterialen maken het vervaardigen van optische verbindingen eenvoudiger
Nieuwe polymeermaterialen maken het vervaardigen van optische verbindingen eenvoudiger
 Caribische eilanden worden geconfronteerd met verlies van bescherming en biodiversiteit omdat zeegras terrein verliest
Caribische eilanden worden geconfronteerd met verlies van bescherming en biodiversiteit omdat zeegras terrein verliest Economische impact van kusterosie
Economische impact van kusterosie  Beïnvloedt de mate van seksuele dimorfisme bij een soort evolutie van die soort?
Beïnvloedt de mate van seksuele dimorfisme bij een soort evolutie van die soort?  Waar is een jungle?
Waar is een jungle?  Welke menselijke activiteiten hebben een negatief effect op de oceaan?
Welke menselijke activiteiten hebben een negatief effect op de oceaan?
Hoofdlijnen
- Masterchef-techniek blijkt levensreddend te zijn voor bedreigde zeeschildpadeieren
- Hoe meer leren over massale nesten kan helpen bij het behoud van zeeschildpadden
- Welke definitie wordt gebruikt om instrumenten in te delen in de classificatie van idiofoon?
- Zijn microplastics alomtegenwoordig in het Nigeriaanse drinkwater?
- Wat is eukaryotische cel?
- Door alles te proberen, leert de roofzuchtige zeeslak wat hij niet mag eten
- Uitvindingen van de evolutie:wat kikkers een gezicht geeft
- Wat wordt elke cel omgeven die het interieur van zijn omgeving scheidt?
- Welk molecuul heeft Carl Woese bestudeerd om zijn levensboom te produceren?
- Wetenschappers creëren een niet-psychedelische verbinding met hetzelfde antidepressieve effect
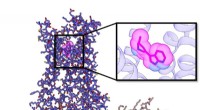
- Katalytische reacties beheersen door nano-oppervlakken te veranderen

- Kenniskloof gedicht in ons begrip van degradatie van ethaan
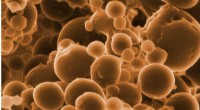
- Wetenschappers ontdekken nieuwe aanwijzing achter ouderdomsziekten en voedselbederf
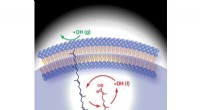
- Video:Waarom plastic flessen worden gerecycled tot kleding

 Wonder of luchtspiegeling? Atmosferische rivieren eindigen het droogtejaar in Californië met zware sneeuwval en regen
Wonder of luchtspiegeling? Atmosferische rivieren eindigen het droogtejaar in Californië met zware sneeuwval en regen  Hoeveel golven passeren er in een bepaalde seconde?
Hoeveel golven passeren er in een bepaalde seconde?  Ga naar het westen, jonge den:Amerikaanse bossen verschuiven door klimaatverandering
Ga naar het westen, jonge den:Amerikaanse bossen verschuiven door klimaatverandering Onderzoek toont raciale stereotypering ten aanzien van jonge kinderen aan
Onderzoek toont raciale stereotypering ten aanzien van jonge kinderen aan Hoe de bevoorradingsspecialisten van legereenheden werken
Hoe de bevoorradingsspecialisten van legereenheden werken  Welke opdringerige stollingsrots heeft dezelfde minerale compositie als basalt?
Welke opdringerige stollingsrots heeft dezelfde minerale compositie als basalt?  Wat is het diagram voor elektrische lay -out?
Wat is het diagram voor elektrische lay -out?  Studie vindt delta helpt de impact van rivieroverstromingen te verminderen
Studie vindt delta helpt de impact van rivieroverstromingen te verminderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

