
Wetenschap
Covalente bindingen en polariteit:polariseren alle covalente moleculen?
Dit is waarom:
* Polariteit ontstaat door ongelijkmatige verdeling van elektronen. Covalente bindingen ontstaan wanneer atomen elektronen delen. Als de elektronen gelijkelijk worden gedeeld, is de binding niet-polair. Als één atoom de gedeelde elektronen dichter naar zich toe trekt, wordt de binding polair.
* Elektronegativiteit bepaalt de polariteit. Elektronegativiteit is het vermogen van een atoom om elektronen aan te trekken. Hoe groter het verschil in elektronegativiteit tussen twee gebonden atomen, hoe polairder de binding.
* Moleculaire geometrie speelt ook een rol. Zelfs als een molecuul polaire bindingen heeft, kan het totale molecuul niet-polair zijn als de polaire bindingen symmetrisch zijn gerangschikt, waardoor de dipoolmomenten worden opgeheven.
Voorbeelden:
* Niet-polaire covalente moleculen:
* CO2 (kooldioxide): De twee C=O-bindingen zijn polair, maar de lineaire vorm van het molecuul zorgt ervoor dat de polariteiten elkaar opheffen.
* CH4 (methaan): De C-H-bindingen zijn enigszins polair, maar de tetraëdrische vorm van het molecuul maakt het niet-polair.
* Polaire covalente moleculen:
* H2O (water): De O-H-bindingen zijn zeer polair en de gebogen vorm van het molecuul zorgt ervoor dat de polariteiten niet worden opgeheven.
* NH3 (ammoniak): De NH-bindingen zijn polair en de piramidevorm van het molecuul maakt het polair.
Samenvattend is een covalente binding een vereiste voor polariteit, maar het is niet de enige factor. Het elektronegativiteitsverschil tussen atomen en de moleculaire geometrie dragen allemaal bij aan het bepalen of een molecuul polair of niet-polair is.
 Milieuvriendelijke technologie om energie te produceren uit textielafval
Milieuvriendelijke technologie om energie te produceren uit textielafval Vijf manieren waarop kunst kan helpen de plasticcrisis op te lossen
Vijf manieren waarop kunst kan helpen de plasticcrisis op te lossen Duurzame landbouw:opbrengst garanderen en broeikasgassen verminderen
Duurzame landbouw:opbrengst garanderen en broeikasgassen verminderen De kenmerken en fysieke kenmerken van een Tiger
De kenmerken en fysieke kenmerken van een Tiger Onderzoekers ontwikkelen app om gebieden te detecteren die het meest kwetsbaar zijn voor levensbedreigende waas
Onderzoekers ontwikkelen app om gebieden te detecteren die het meest kwetsbaar zijn voor levensbedreigende waas
Hoofdlijnen
- Wat US Baptisim?
- Wat is de celkern voor broodvorm?
- Wat is een schimmel die sporen schiet?
- Welke cel helpt de plant de vorm te behouden?
- Hoe goed worden alternatieve eiwitbronnen ontvangen door de eindconsument?
- De enzymen die chemische reacties in levende wezens katalyseren, zijn één type?
- Beschrijf het DNA -model dat je hebt geconstrueerd?
- Wat is afvalverwijdering in een cel?
- Hoe wordt SAC gevormd uit stukken celmembraan?
- CRISPR ontgint bacterieel genoom voor verborgen farmaceutische schat

- Een thermometer die kan worden uitgerekt en vervormd door water
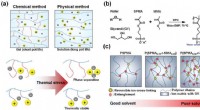
- Nieuw upcycling-systeem voor commerciële polyesters

- Nog een reden om van de gestreepte bas te houden:antimicrobiële middelen

- Een nieuwe manier om met zonlicht schone waterstofbrandstof te maken uit water

 Wat brengt een golfoverdracht als de deeltjes zelf niet bewegen?
Wat brengt een golfoverdracht als de deeltjes zelf niet bewegen?  Van gegevens tot beslissingen:AI en IoT voor het voorspellen van aardbevingen
Van gegevens tot beslissingen:AI en IoT voor het voorspellen van aardbevingen  Ozonaantasting verhoogt Antarctische sneeuwval, vermindert gedeeltelijk het verlies van ijskappen
Ozonaantasting verhoogt Antarctische sneeuwval, vermindert gedeeltelijk het verlies van ijskappen Afbeelding:Gigantische magnetische touwen in een halo van sterrenstelsels
Afbeelding:Gigantische magnetische touwen in een halo van sterrenstelsels Wat is de geografische locatie van graniet?
Wat is de geografische locatie van graniet?  Ondersteuning van de vorm van een hele cel?
Ondersteuning van de vorm van een hele cel?  Is de iPhone zoals privé Apple zegt? Mozilla zegt dat dit mogelijk is
Is de iPhone zoals privé Apple zegt? Mozilla zegt dat dit mogelijk is  Wat is het doel van chemische zender in een besturingssysteem?
Wat is het doel van chemische zender in een besturingssysteem?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

