
Wetenschap
Valentie-elektronen en atomaire stabiliteit:de octetregel begrijpen
Dit is waarom:
* Valentie-elektronen: Dit zijn de elektronen in de buitenste schil van een atoom. Zij zijn degenen die betrokken zijn bij chemische binding.
* Stabiliteit: Atomen zijn het meest stabiel als hun buitenste schil gevuld is met elektronen. Dit komt omdat een gevulde schaal energetisch gunstig is.
* Octet-regel: Voor de meeste elementen bevat een volledige buitenschil 8 elektronen. Dit is de reden waarom atomen de neiging hebben elektronen te winnen, te verliezen of te delen om deze configuratie te bereiken.
Voorbeelden:
* Natrium (Na): Heeft 1 valentie-elektron. Het wil dit elektron kwijtraken om stabiel te worden en een +1-ion te vormen met een volledige buitenschil.
* Chloor (Cl): Heeft 7 valentie-elektronen. Het wil 1 elektron winnen om stabiel te worden en een -1 ion te vormen met een volledige buitenschil.
* Zuurstof (O): Heeft 6 valentie-elektronen. Het wil 2 elektronen verkrijgen om stabiel te worden en een -2-ion te vormen met een volledige buitenschil.
Houd er rekening mee dat de octetregel een generalisatie is en dat er uitzonderingen zijn, vooral bij overgangsmetalen en grotere atomen.
 Welke 2 zijn meer reactief uit siliciumfosfor zwavelchloor germanium arseen selenium broom?
Welke 2 zijn meer reactief uit siliciumfosfor zwavelchloor germanium arseen selenium broom?  Hoe worden de gevormde geladen deeltjes genoemd?
Hoe worden de gevormde geladen deeltjes genoemd?  Een waterige oplossing van natriumchloride kan het best worden geclassificeerd als een wat?
Een waterige oplossing van natriumchloride kan het best worden geclassificeerd als een wat?  Waarom is puim poreus?
Waarom is puim poreus?  Video:Waarom je geen verse olijven kunt kopen
Video:Waarom je geen verse olijven kunt kopen
 Welke bron zou het meest geloofwaardig zijn om te gebruiken in een onderzoekspaper over de omgeving?
Welke bron zou het meest geloofwaardig zijn om te gebruiken in een onderzoekspaper over de omgeving?  Welke planten zijn nauw verwant aan marihuana?
Welke planten zijn nauw verwant aan marihuana?  Firefall-fenomeen verbaast bezoekers aan Yosemites El Capitan
Firefall-fenomeen verbaast bezoekers aan Yosemites El Capitan Landrechten essentieel om biodiversiteit en inheemse culturen te beschermen
Landrechten essentieel om biodiversiteit en inheemse culturen te beschermen Wat zijn de goede en slechte dingen over de wetenschap?
Wat zijn de goede en slechte dingen over de wetenschap?
Hoofdlijnen
- Waarom zijn virussen moeilijk te cultiveren in het laboratorium?
- Dode vissen blazen nieuw leven in de evolutionaire oorsprong van vinnen en ledematen
- Om een kenmerk van de ene soort over te dragen, is het noodzakelijk transfe?
- Hoe je kleding microvezelvervuiling in de zee wordt
- Wat is het proces dat plaatsvindt in groene cellen in organellen genoemd?
- Welke 3 dingen vormen het endomembraantransportsysteem in een cel?
- Wat is een spoel van mitochondria?
- Ontbreekt een van de cellen een celmembraan?
- Wat kan vrijelijk rondzweven in een bacterie maar geen bloem?
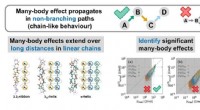
- Wanneer zijn veellichaamseffecten significant?
- Methanol versus isopropylalcohol:belangrijkste verschillen verklaard

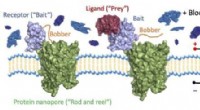
- Wetenschappers ontwikkelen moleculaire visserij om individuele moleculen in bloed te vinden
- Zou de hitte van de aardkorst de ultieme energiebron kunnen worden?

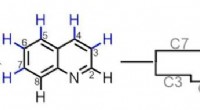
- Chemici bereiken moleculaire bewerkingsprestatie
 Vind het koppel van een kracht 7i plus 3J-5K over oorsprong de handelingen op deeltjes wiens positievector is je-j k?
Vind het koppel van een kracht 7i plus 3J-5K over oorsprong de handelingen op deeltjes wiens positievector is je-j k?  Hoe kan ik een telescoop gebruiken om planeten aan de nachtelijke hemel te zien?
Hoe kan ik een telescoop gebruiken om planeten aan de nachtelijke hemel te zien?  Wat veroorzaakt gaten in stollingsgesteente?
Wat veroorzaakt gaten in stollingsgesteente?  Syngenta schikt Amerikaanse boerenrechtszaken in Chinese maïshandelzaak
Syngenta schikt Amerikaanse boerenrechtszaken in Chinese maïshandelzaak Als een vloeistof een hoge viscositeit heeft, wat betekent dat dan?
Als een vloeistof een hoge viscositeit heeft, wat betekent dat dan?  Hoe hebben wetenschappers Albert Quation E toegepast, is gelijk aan MC2?
Hoe hebben wetenschappers Albert Quation E toegepast, is gelijk aan MC2?  Wat is de stralingswet van Stefan-Boltzmann?
Wat is de stralingswet van Stefan-Boltzmann?  Hoe wordt het genoemd als vloeistof verandert in een gas?
Hoe wordt het genoemd als vloeistof verandert in een gas?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

